
如图装置中, U形管内为红墨水,a、b试管内分别盛有 (显中性的)食盐水和(显酸性的)氯化铵溶液,各加入生铁(含C、Fe)块,a、 b中均能构成原电池而使铁分别被O2和H+ 腐蚀,放置一段时间 。下列有关描述错误的是
。下列有关描述错误的是
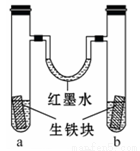
A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式是:Fe-2e- ===Fe2+
D.a试管中O2得电子,b试管中H+ 得电子
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015-2016学年河北省唐山市高一下学期期中理科化学试卷(解析版) 题型:选择题
下列叙述中,能证明A金属比B金属活动性强的是( )
A.A原子的最外层电子数比B原子的最外层电子数少
B.A原子的电子层数比B原子电子层数多
C.1 mol A从酸中置换出的H2比1 mol B从酸中置换出的H2多
D.常温时,A能从冷水中置换出H2,而B不能
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.构成原电池的正极和负极的材料必须是两种金属
B.由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极
C.马口铁(镀锡铁)破损时与电解质溶液接触时锡先被腐蚀
D.铜锌原电池工作时,若有13 g锌被溶解,电路中就有0.4 mol电子通过
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷(解析版) 题型:选择题
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中, 破坏1 mol 氢气中的化学键消耗的能量为Q1 kJ, 破坏1 mol 氯气中的化学键消耗的能量为Q2 kJ, 形成1 mol 氯化氢中的化学键释放的能量为Q3 kJ。下列关系式中,正确的是
A.Q1+Q2>Q3 B.Q1+Q2>2Q3 C.Q1+Q2<Q3 D.Q1+Q2<2Q3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省秦皇岛市卢龙县高一下学期期中考试化学试卷(解析版) 题型:选择题
第十一届中国国际环保展览暨会议于2009年6月3日至6日在北京举行。海外展商有包括美国、法国的23个国家和地区。大会主题是“节能减排,和谐发展。”你认为下列行为中有悖于这一主题的是
A.开发太阳能、水能、风能、可燃冰等新能源,减少使用煤、石油等化石燃料
B.将煤进行气化处理,提高煤的综合利用效率
C.研究采煤、采油新技术,提高产量以满足工业生产的快速发展
D.实现资源的“3R”利用观,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、资源的循环再生(Recycle)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市大名等四县高二下学期期中联考化学试卷(解析版) 题型:选择题
向一定量的Fe、FeO和Fe2O3的混合物中加入120 mL 4 mol·L-1的稀硝酸,恰好使混合物完全溶解,放出1.344 L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为( )
A.0.24 mol B.0.21 mol C.0.16 mol D.0.14 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下学期期中考试化学试卷(解析版) 题型:实验题
为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验
Ⅰ.以H2O2的分解反应为研究对象,实验方案与数据记录如下表,t表示收集a mL O2所需的时间。
序号 | 反应 温度/℃ | c(H2O2)/ mol·L-1 | V(H2O2) /mL | m(MnO2) /g | t/min |
1 | 20 | 2 | 10 | 0 | t1 |
2 | 20 | 2 | 10 | 0.1 | t2 |
3 | 20 | 4 | 10 | 0.1 | t3 |
4 | 40 | 2 | 10 | 0.1 | t4 |
(1)设计实验2和实验3的目的是研究________________________对化学反应速率的影响。
(2)为研究温度对化学反应速率的影响,可以将实验________和实验________(填序号)作对比。
(3)将实验1和实验2作对比,t1________t2(填“>”、“<”或“=”)。
Ⅱ.以KI和FeCl3反应为例(2Fe3++2I-===2Fe2++I2)设计实验,探究此反应存在一定的限度。可选试剂:①0.1 mol·L-1 KI溶液 ②0.1 mol·L-1 FeCl3溶液
③0.1 mol·L-1 FeCl2溶液 ④0.1 mol·L-1 盐酸
⑤0.1 mol·L-1 KSCN溶液 ⑥CCl4
实验步骤:(1)取5 mL 0.1 mol·L-1 KI溶液,再滴加几滴0.1 mol·L-1 FeCl3溶液
(2)充分反应后,将溶液分成三份
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘
(4)另取一份,加试剂________(填序号),现象________________________,说明此反应存在一定的限度。
Ⅲ.N2O4可分解为NO2。在100 mL密闭容器中投入0.01 mol N2O4,利用现代化学实验技术跟踪测量c(NO2)。c(NO2)随时间变化的数据记录如下图所示。

(1)反应容器中最后剩余的物质有________________,其中N2O4的物质的量为________mol。
(2)c(NO2)随时间变化的曲线表明,实验测得的化学反应速率在逐渐减小,从开始到平衡建立这段时间的平均反应速率为________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄石市高一下学期期中考试化学试卷(解析版) 题型:选择题
下列溶液中,不能区别SO2和CO2气体的是( )
①石灰水 ②H2S溶液 ③KMnO4溶液 ④溴水 ⑤酸化的Ba(NO3)2 溶液 ⑥品红溶液
A.①②③⑤ B.②③④⑤ C.只有① D.①⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com