
| ① | ② | ③ | ④ | ⑤ |
| 0.001mol?L-1 CH3COOH溶液 | pH=10 NaOH溶液 | 0.001mol?L-1 NaOH溶液 | pH=4 CH3COOH溶液 | pH=4 NH4Cl溶液 |


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
 如图a、b、c、d均为石墨电极,通电进行电解.下列说法不正确的是( )
如图a、b、c、d均为石墨电极,通电进行电解.下列说法不正确的是( )| A、甲中a电极反应式为4OH--4e-=O2↑+2H2O |
| B、电解后向乙中通入适量HCl气体,溶液组成可以恢复 |
| C、当b极有64gCu析出时,c电极产生2g气体 |
| D、电解时向乙中滴入酚酞试剂,d电极附近变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol P4中P-P键的数目为6NA |
| B、1mol Na2O2晶体中含有阴阳离子总数为4NA |
| C、30g SiO2晶体中含有Si-O键数目为2NA |
| D、6g金刚石中含有的碳碳键数目为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
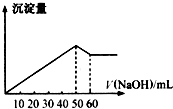 (1)在某Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为
(1)在某Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质发生化学变化并不一定都伴随着能量变化 |
| B、用实验方法和理论方法研究反应热的化学称为热化学 |
| C、只要有能量变化的都是化学变化 |
| D、任何反应中的能量变化都表现为热量变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com