
【题目】锂离子电池己被广泛用作便携式电源。正极材料为LiCoO2、LiFePO4等,负极材料一般为石墨碳,以溶有LiPF6、LiBF4等的碳酸二乙酯(DEC)作电解液。
(1)Fe2+基态核外电子排布式为 ________。
(2)PO43-的空间构型为 ________ (用文字描述)。
(3)![]() 中
中![]() 的配位数为6,该配合物中的配位原子为 _____。
的配位数为6,该配合物中的配位原子为 _____。
(4)碳酸二乙酯(DEC)的分子结构如图所示,分子中碳原子的轨道杂化类型为_____,1mol碳酸二乙酯(DEC)中含有σ键的数目为_____。
![]()
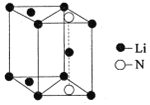
(5)氮化锂是一种新型无机贮氢材料,其晶胞结构如图所示,该晶体的化学式为_______。
【答案】![]() 正四面体 N、Cl sp3、sp2 17NA Li3N
正四面体 N、Cl sp3、sp2 17NA Li3N
【解析】
(1)Fe2+原子核外有24个电子,依据核外电子排布规律, Fe2+基态核外电子排布式为![]() ,
,
故答案为:![]() ;
;
(2)P原子孤电子对数![]() ,价层电子对数
,价层电子对数![]() ,故PO43-的空间构型为正四面体,
,故PO43-的空间构型为正四面体,
故答案为:正四面体;
(3)![]() 中
中![]() 的配位数为6,则配体为Cl和NH3,配位原子为Cl、N,
的配位数为6,则配体为Cl和NH3,配位原子为Cl、N,
故答案为:N、Cl;
(4)根据碳酸二乙酯(DEC)的分子结构示意图可知,碳酸二乙酯中含有酯键,和甲基团,故碳原子的轨道杂化类型为sp3、sp2;碳酸二乙酯中含有17个σ键和一个π键,故1mol碳酸二乙酯(DEC)中含有σ键的数目为17NA,
故答案为:sp3、sp2;17NA;
(5)通过晶胞结构图可知Li原子数![]() ,N原子数
,N原子数![]() ,故化学式为Li3N,
,故化学式为Li3N,
故答案为:Li3N。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】常温下向10mL0.1mol/L的NaCN溶液中滴加等浓度的盐酸(忽略体积和温度变化),δ(HCN)和![]() 随溶液pH变化的图像如图所示,下列说法错误的是
随溶液pH变化的图像如图所示,下列说法错误的是
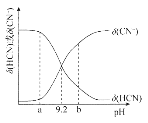
A.常温下HCN的电离常数为l0-9.2
B.pH为9.2时,加入盐酸的体积大于5mL
C.pH为a时溶液中c(Cl-)大于pH为b时溶液中c(Cl-)
D.滴加过程中可能出现:c(Na+)>c(CN-)>c(OH-)>c(Cl-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
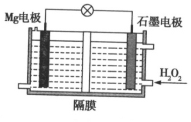
【题目】![]() 电池可用于驱动无人潜航器。该电池以海水为电解质溶液,如图所示。该电池工作时,下列说法正确的是 ( )
电池可用于驱动无人潜航器。该电池以海水为电解质溶液,如图所示。该电池工作时,下列说法正确的是 ( )
A.电池总反应是![]()
![]()
![]()
B.![]() 在石墨电极上反应放出氧气
在石墨电极上反应放出氧气
C.石墨电极附近溶液的pH增大
D.溶液中![]() 向正极移动
向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液的pH通常在7.35-7.45之间的原因是血液中存在NaH2PO4-Na2HPO4等缓冲体系。常温下:Ka1(H3PO4)=7.6×10-3、Ka2(H3PO4)=6.3×10-8。下列指定溶液中微粒物质的量浓度关系正确的是
A.0.1mol/L NaH2PO4溶液:2c(HPO42-)+3c(PO43-)>c(Na+)-c(H2PO4-)
B.常温下,pH=7的NaH2PO4和Na2HPO4的混合溶液:c(Na+)>c(HPO42-)>c(H2PO4-)
C.向10 mL0.1mol/L NaH2PO4溶液中加入5mL 0.4 mol/L NaOH溶液:c(H+)+3c(H3PO4)+2c(H2PO4-)+c(HPO42-)=c(OH-)
D.物质的量浓度相等NaH2PO4和Na2HPO4溶液等体积混合:3[c(H2PO4-)+c(HPO42-)+c(PO43-)]=2c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以含银废液{主要含[Ag(NH3)2]+、[Ag(S2O3)2]3-}为原料制取硝酸银晶体,其实验流程如下:

已知:①“沉银”所得AgCl中含有少量PbCl2、Ag2S。
②Zn2+在浓氨水中以[Zn(NH3)4]2+形式存在。
③PbCl2、AgNO3的溶解度曲线如图所示:

(1)“滤液”中的主要阳离子为___(填化学式)。
(2)“除杂”分为两步:先除去PbCl2,再除去Ag2S。
①在不同温度下,AgCl、Ag2S均难溶于水。 除去PbCl2的操作为______,热水洗涤。
②向热水洗涤所得固体中加入浓硝酸和稀盐酸,边加热边充分搅拌,使Ag2S转变为AgCl。加入浓硝酸的目的是_______。
(3)室温下,可逆反应AgCl+2NH3·H2O[Ag(NH3)2]++Cl-+2H2O的平衡常数K=___。{Ksp(AgCl)= 1.8×10-10,Ag++2NH3·H2O[Ag(NH3)2]++2H2O的平衡常数为1.1×107}
(4)“还原”过程中发生反应的离子方程式为_____ 。
(5)粗银经水洗后,经多步处理可制备硝酸银晶体。请补充完整由以水洗后粗银为原料,制备硝酸银晶体的实验方案:________,过滤,________,将产生的气体和空气混合后通入NaOH溶液进行尾气处理,将所得AgNO3溶液_______,过滤,将所得晶体置于烘箱 (120℃)干燥,密封包装。(实验中须使用的试剂:稀硫酸、稀硝酸、BaC12溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是( )
A.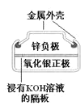 正极的电极反应式为Ag2O+2e-+H2O=2Ag+2OH-
正极的电极反应式为Ag2O+2e-+H2O=2Ag+2OH-
B. 锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
C.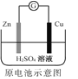 Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
D.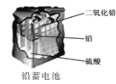 使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是:600℃ 时,在2L密闭容器里A、B、C三种气体在密闭容器中反应时浓度的变化,其中A为有色气体,B、C是无色气体。请从图中分析并填空:
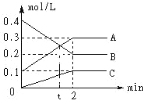
(1)该反应的化学反应方程式为_____
(2)反应达到平衡状态时,反应物的转化率为_____
(3)当反应进行到第_____min,该反应达到平衡。
(4)反应从开始至2分钟末,B的物质的量_____,用B的浓度变化表示的平均反应速率为v(B)=_
(5)下列描述能表示反应达平衡状态的是_____(填选项)。
a.容器中A与B的物质的量相等
b.容器内气体的颜色不再改变
c.各物质的浓度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z 三种物质的物质的量随时间的变化曲线如图所示。
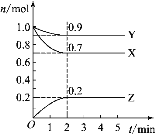
(1)由图中数据分析,该反应的化学方程式_____________。
(2)从反应开始至2 min,Z的平均反应速率为________。
(3)第5 min时,Z的生成速率________(填“大于”“小于”或“等于”)Z的消耗速率。
(4)第_______分钟时,反应达到平衡。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com