

分析 (1)装置A中二氧化锰与浓盐酸子在加热条件下反应生成氯化锰、氯气和水;
(2)浓盐酸易挥发,加热能够促进氯化氢的挥发,所以制备的氯气中含有氯化氢和水蒸气,要制备纯净干燥的氯气,应除去氯化氢和水蒸气,结合氯化氢、氯气的溶解性、浓硫酸的吸水性解答;
(3)氯气有毒,直接排放能够引起空气污染,氯气能够与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,可以用氢氧化钠溶液吸收过量的氯气;
(4)因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,所以F中试剂为浓硫酸防止水蒸气进入E收集瓶.
解答 解:(1)二氧化锰与浓盐酸子在加热条件下反应生成氯化锰、氯气和水,化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)浓盐酸易挥发,加热能够促进氯化氢的挥发,所以制备的氯气中含有氯化氢和水蒸气,要制备纯净干燥的氯气,应除去氯化氢和水蒸气,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,选用盛有饱和食盐水的洗气瓶除去氯气中的氯化氢,浓硫酸具有吸水性能够干燥氯气;
故答案为:饱和食盐水; 除去Cl2中的HCl气体;浓H2SO4; 干燥Cl2(或除去Cl2中的水蒸气);
(3)氯气有毒,直接排放能够引起空气污染,氯气能够与氢氧化钠溶液反应,化学方程式为:Cl2+2NaOH═NaCl+NaClO+H2O,可以用氢氧化钠溶液吸收过量的氯气,所以装置G作用为:吸收多余的Cl2,防止污染环境;
故答案为:吸收多余的Cl2,防止污染环境;Cl2+2NaOH═NaCl+NaClO+H2O;
(4)因为氯化铝易发生水解,故应该防止空气中的水蒸气进入E装置,所以F中试剂为浓硫酸防止水蒸气进入E收集瓶;
故答案为:浓H2SO4;吸收水蒸气,防止G中水蒸气进入E中使AlCl3遇潮产生白雾.
点评 本题考查了氯化铝的制备工艺,侧重考查学生对于工艺流程原理的理解、对操作与实验条件控制的理解,明确氯气制备原理、氯化铝的性质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 用浓盐酸检验氨:NH3+HCl═NH4Cl | |
| B. | 切开的金属Na暴露在空气中,光亮表面逐渐变暗4Na+O2═2Na2O | |
| C. | Na2O2在潮湿空气中放置一段时间,变成白色粘稠物2Na2O2+2CO2═2Na2CO3+O2 | |
| D. | 长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 s末氨气的反应速率=0.4 mol•(L•s)-1 | |
| B. | 前2 s时间内氢气的平均反应速率=0.9 mol•(L•s)-1 | |
| C. | 前4 s时间内氮气的平均反应速率=0.1mol•(L•s)-1 | |
| D. | 2~4 s时间内氨气的平均反应速率=0.2 mol•(L•s)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1mol/L•min | B. | 1.5mol/L•min | C. | 0.5mol/L•min | D. | 3mol/L•min |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2 CH2 | B. | CS2分子的结构式:S═C═S | ||
| C. | 醛基的结构简式:-CHO | D. | 羟基的电子式:${\;}_{\;}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$H |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



 .写出A与溴水的反应方程式
.写出A与溴水的反应方程式 +3Br2→
+3Br2→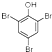 ↓+3HBr
↓+3HBr 或
或 (任写一个).
(任写一个). .
. 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁在空气中燃烧发出耀眼的白光,可用于制作照明弹 | |
| B. | 在一定条件下可实现下列转化MgCl2(溶液)→Mg(OH)2→MgO | |
| C. | 通过置换反应可实现由Mg到MgO的转化 | |
| D. | 镁与稀硝酸反应的离子方程式为:Mg+2H+═Mg+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com