
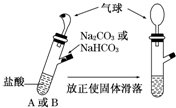
| A. | A装置的气球膨胀速度快 | |
| B. | 若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol/L | |
| C. | 若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol/L | |
| D. | 最终两试管中Na+的物质的量一定相同 |
分析 A.碳酸钠先与氢离子反应生成碳酸氢钠,碳酸氢钠与氢离子反应生成二氧化碳气体,所以碳酸氢钠产生氢气速率大于碳酸钠;
B.由于Na2CO3和NaHCO3的物质的量相同,若最终两气球体积相同,说明酸的物质的量大于或等于0.02mol,据此判断盐酸浓度;
C.产生相同体积的二氧化碳时消耗0.02mol氢离子,据此判断盐酸的浓度;
D.碳酸钠和碳酸氢钠的物质的量相等,则钠离子的物质的量不相等.
解答 解:A.碳酸钠和酸反应分步进行,先生成碳酸氢钠,后碳酸氢钠和盐酸反应生成二氧化碳,所以A装置的气球膨胀速率慢,故A错误;
B.Na2CO3和NaHCO3的物质的量相同,若最终两气球体积相同,说明酸的物质的量大于或等于0.02mol,所以其浓度大于或等于2mol/,故B正确;
C.碳酸钠和酸反应的离子方程式为:CO32-+H+=HCO3-、HCO3-+H+=CO2↑+H2O,碳酸氢钠和酸反应的离子方程式为HCO3-+H+=CO2↑+H2O,若最终两气球体积不同,所需酸的物质的量范围是:0<酸的物质的量<0.02mol,所以其浓度大于0小于2mol/L,故C错误;
D.0.01molNa2CO3和0.01molNaHCO3的物质的量相等,所以Na2CO3和 NaHCO3中钠离子的物质的量不同,故最终两试管中Na+的物质的量一定不相同,故D错误;
故选B.
点评 本题考查了碳酸钠和碳酸氢钠的性质,题目难度中等,碳酸钠和酸反应分步进行,先生成碳酸氢钠,后碳酸氢钠和酸反应生成二氧化碳,试题培养了学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | Pb2++2CH3COO-+2H++S2-═PbS↓+2CH3COOH | |
| B. | Pb2++H2S═PbS↓+2H+ | |
| C. | Pb2++2CH3COO-+H2S═PbS↓+2CH3COOH | |
| D. | (CH3COO)2Pb+H2S═PbS↓+2CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
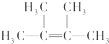 ;名称是2,3-二甲基-2-丁烯.
;名称是2,3-二甲基-2-丁烯.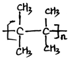 .
.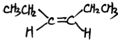 或(CH3CH2)2C=CH2.
或(CH3CH2)2C=CH2.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
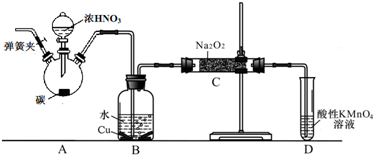
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(SO2)/mol |
| 0 | 2.0 | 2.0 | 0 |
| 2 | 0.8 | ||
| 4 | 1.2 | ||
| 6 | 1.2 | 2.8 |
| A. | 0~2 min内的平均速率为υ(CO)=0.6mol/(L•min) | |
| B. | 4min后,平衡移动的原因可能是向容器中加入了2.0mol的SO2 | |
| C. | 若升高温度,反应的平衡常数变为1.0,则正反应为放热反应 | |
| D. | 其他条件不变,若起始时容器中MgSO4、CO均为1.0mol,则平衡时n(SO2)=0.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3的质量分数将增加 | B. | 平衡向正反应方向移动 | ||
| C. | 平衡向逆反应方向移动 | D. | 正逆反应速率都增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
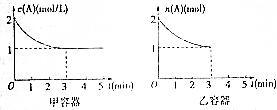
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
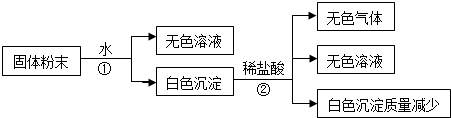
| 序号 | 化 学 式 |
| Ⅰ | |
| Ⅱ | |
| Ⅲ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5L1.2mol•L-1的Na2SO4溶液 | B. | 2L 0.8mol•L-1的Na0H溶液 | ||
| C. | 1L1mol•L-1的Na2CO3溶液 | D. | 4L 0.5mol•L-1的NaCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com