
(08东莞调研)(10分)二元酸H2A的电离反应如下:
H2A ![]() HA- + H+ K1 = 4.50×10-7 HA-
HA- + H+ K1 = 4.50×10-7 HA-![]() A2- + H+ K2 = 4.70×10-11
A2- + H+ K2 = 4.70×10-11
用0.300 mol?L-1 HCl滴定含有Na2A和NaHA的一份20.00 mL的溶液,滴定进程用玻璃电极pH计跟踪,滴定曲线上的三个点对应的数据如下:
加入的HCl/mL | 1.00 | 10.00 | 28.00 |
pH | 10.33 | 8.34 | 6.35 |
(1)加入1.00 mL HCl时首先与HCl反应的溶质是 ,产物是 。
(2)(1)中生成的产物有 mol。
(3)写出(1)中生成的产物与溶剂反应的主要平衡式: 。
(4)当pH=8.34时反应混合物有两种溶质,而pH=6.35时反应混合物只有一种含钠化合物溶质,试计算起始溶液中存在的Na2A和NaHA的物质的量浓度?(忽略溶质的水解与电离,写出计算过程)
答案:(1)A2-,HA-(各1分)
(2)0.300 ×10-4mol(2分)
(3)HA- + H2O ![]() H2A + OH-(2分)
H2A + OH-(2分)
(4)解:当pH=8.34时反应混合物有两种溶质,则溶液中有NaCl和NaHA;
反应为 A2- + H+= HA-
1 mol 1 mol 1 mol
3.00×10-3 mol 0.3000 mol?L-1×10.00×10-3 L 3.00×10-3 mol
C(Na2A)= 3.00×10-3 mol /20.00×10-3 L= 0.15 0mol?L-1(3分)
pH=6.35时反应混合物只有一种含钠化合物溶质, 则溶液中有NaCl和H2A;
反应为 HA-+ H+= H2A
1 mol 1 mol 1 mol
5.40×10-3 mol 0.3000 mol?L-1×(28.00-10.00)×10-3 L 5.40×10-3 mol
CNaHA)=( 5.40×10-3-3.00×10-3) mol/20.00×10-3 L =0.120mol?L-1(3分)


科目:高中化学 来源: 题型:
(08东莞调研)实验室现有下列药品:①蒸馏水;②用HNO3酸化的AgNO3溶液;③熟石灰;④Na2CO3;⑤NaCl;⑥食醋;⑦废干电池(锌筒内填有炭粉、MnO2、NH4Cl、淀粉等糊状物)。某课外兴趣小组同学准备进行下列实验研究:
(1)利用上述药品制NaOH溶液的化学方程式是 。
(2)为制备NH3,可先从废干电池中制备NH4Cl。假设将废电池中的混合物溶于少量的水中,过滤除去不溶物,再蒸发滤液,并灼烧以制得干燥的NH4Cl晶体。你认为这一设想是否合理?答: ,其理由是 。
(3)他们在进行除去淀粉溶液中食盐的实验时,用鸡蛋壳膜自制了一个半透膜小袋,向其中装入混有NaCl的淀粉溶液,扎好袋口,这一实验的操作名称为 。要保证全部除去淀粉溶液里的食盐,实验中必须 。
(4)由于实验(2)中NH4Cl的制备较困难,且难以满足量的要求,现重新提供足量的浓氨水、浓NaOH溶液和NH4Cl晶体,请设计一个最简单的实验,以快速制得NH3。
①你设计的实验方案是 。
②请运用化学原理对你的方案予以解释 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08东莞调研)将0.2mol?L-1 HA溶液与0.2mol?L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则(用“>”、“<”或“=”填写下列空白)
(1)混合溶液中c(HA)_______c(A-);
(2)混合溶液中c(HA)+c(A-)______0.1mol?L-1;
(3)混合溶液中,由水电离出的c(OH-)______0.2mol?L-1HA溶液由水电离出的c(H+);
(4)25℃时,如果取0.2mol?L-1 HA溶液与0.11 mol?L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度______NaA的水解程度。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08东莞调研)贫铀炸弹是一种杀伤力很强的武器。贫铀是提炼铀235后的副产品,其主要成分是铀238。贫铀炸弹不仅有很强的穿甲能力,而且铀238具有放射性,人长期受到核辐射会患皮肤癌和白血病。以下关于铀元素的叙述正确的是( )
A. 23892U原子中中子数比核外电子数多146个
B. 23892U和 23592U互为同素异形体
C.铀元素位于元素周期表的第六周期
D.铀元素属于过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
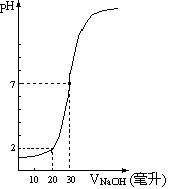 (08东莞调研)下图为10mL一定物质的量浓度的盐酸X,用一定物质的量浓度的NaOH溶液Y滴定的图示,据图推出NaOH溶液和盐酸的物质的量的浓度是( )
(08东莞调研)下图为10mL一定物质的量浓度的盐酸X,用一定物质的量浓度的NaOH溶液Y滴定的图示,据图推出NaOH溶液和盐酸的物质的量的浓度是( )
| A | B | C | D |
C(HCl)(mol/L) | 0.12 | 0.04 | 0.18 | 0.09 |
C(NaOH)(mol/L) | 0.04 | 0.12 | 0.06 | 0.03 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com