
【题目】某同学欲用物质的量浓度为0.100 0 mol·L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液,选择酚酞作指示剂。请填写下列空白:
(1) 用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,直到因加入一滴盐酸,溶液_________________,立即停止滴定。
(2) 下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 (填序号)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出

(3) 若某次滴定结束时,酸式滴定管中的液面如图所示,则读数为 mL。若仰视,会使读数偏___________(填“大”或“小”)。
(4) 再结合下表数据,计算被测氢氧化钠溶液的物质的量浓度是 mol·L-1。
滴定 次数 | 待测溶液 体积/mL | 标准酸体积 | |
滴定前的刻度/mL | 滴定后的刻度/mL | ||
第一次 | 10.00 | 1.34 | 19.39 |
第二次 | 10.00 | 4.10 | 21.10 |
第三次 | 10.00 | 0.40 | 17.60 |
【答案】(1)颜色由浅红变为无色,且半分钟不恢复红色。(2分)
(2)DE(4分) (3)19.12(2分)大(2分) (4)0.1710 (2分)
【解析】
试题分析:(1) 用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,直到因加入一滴盐酸,溶液颜色由浅红变为无色,且半分钟不恢复红色,立即停止滴定。
(2) A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸,导致盐酸浓度降低,消耗盐酸溶液的体积增加,浓度偏高;B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,不会影响实验结果;C.酸式滴定管在滴定前有气泡,滴定后气泡消失,导致消耗盐酸溶液的体积增加,浓度偏高;D.读取盐酸体积时,开始仰视读数,读数偏大,滴定结束时俯视读数,读数偏小,消耗盐酸溶液的体积增加,浓度偏低;E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出,导致消耗盐酸溶液的体积减少,浓度偏低,答案选DE;
(3) 若某次滴定结束时,酸式滴定管中的液面如右图所示,则读数为19.12mL。若仰视,会使读数偏大”或。
(4)三次消耗盐酸溶液的体积为18.05mL、17.00mL、17.20mL,其中第一次实验数据误差太大,舍去,其平均值为17.10mL,因此被测氢氧化钠溶液的物质的量浓度是![]() =0.1710mol·L-1。
=0.1710mol·L-1。


科目:高中化学 来源: 题型:
【题目】在某密闭恒容容器中发生反应:X(g) ![]() Y(g)+nZ(g) ΔH=+QkJ/mol(Q>0)。反应体系2min时达到 平衡后,各物质的浓度在不同条件下的变化如下图所示。(第10min到16min的X浓度变化曲线未标出),下列说法不正确的是
Y(g)+nZ(g) ΔH=+QkJ/mol(Q>0)。反应体系2min时达到 平衡后,各物质的浓度在不同条件下的变化如下图所示。(第10min到16min的X浓度变化曲线未标出),下列说法不正确的是
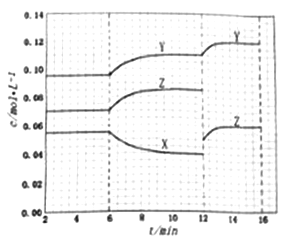
A. 反应方程式中n=1
B. 12min-14min内,用Y表示的评价速率为0.005mol/(L·min)
C. 在6min-10min内,反应吸收的热量为0.015Q kJ
D. 第12min时,Z曲线发生变化的原因是移走一部分Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性:H2SO3>H2CO3>HSO3->HCO3-。某无色溶液Y可能含有Na+、Fe3+、Ba2+、NH4+、Cl-、SO42-、HCO3-、HSO3-中的几种离子,溶液中阳离子浓度相同。为了确定其组成,某同学进行了如下实验(假设气体均全部逸出,忽略H2O2的分解)。
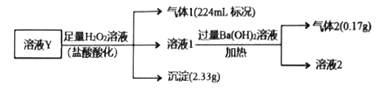
下列说法不正确的是
A. 溶液Y中一定不存在Fe3+、SO42-
B. 溶液Y中肯定存在HCO3-、HSO3-、Ba2+、NH4+
C. 溶液Y中一定含有Cl-,且n(Cl-)=0.01mol
D. 溶液Y中可能存在Na+,为确定其是否存在,可取溶液1通过焰色反应实验验证
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3,两步反应的能量变化示意图如下:

下列说法合理的是( )
A.该反应的催化剂是NO2
B.升高温度,两步反应速率均加快,有利于NH4+ 转化成NO3
C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态
D.1 mol NH4+在第一步反应中与1 mol NO2-在第二步反应中失电子数之比为1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素原子最外层有2个电子,关于此元素的说法一定正确的是( )
A.ⅡA族元素
B.可能是金属元素,也可能是非金属元素
C.金属元素
D.ⅡA族或ⅡB族元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 澄清石灰水跟过量CO2气体反应:Ca(OH)2+CO2=CaCO3↓+H2O
B. 稀硫酸与Cu反应:2H++Cu=Cu2++H2↑
C. 腐蚀法制作印刷线路板:2Fe3++Cu=2Fe2++Cu2+
D. 铁粉加入AgNO3溶液中:Fe+Ag+=Fe2++Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族羧酸通常用芳香烃的氧化来制备。芳香烃的苯环比较稳定,难于氧化,而环上的支链不论长短,在强烈氧化时,最终都氧化成羧基。某同学用甲苯的氧化反应制备苯甲酸。
反应原理:

反应试剂、产物的物理常数:
名称 | 相对分 子质量 | 性状 | 熔点 | 沸点 | 密度 | 溶解度 | ||
水 | 乙醇 | 乙醚 | ||||||
甲苯 | 92 | 无色液体易燃易挥发 | -95 | 110.6 | 0.8669 | 不溶 | 易溶 | 易溶 |
苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 | 248 | 1.2659 | 微溶 | 易溶 | 易溶 |
主要实验装置和流程如下:
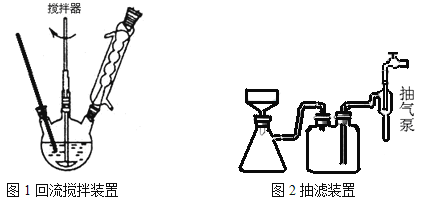
实验方法:一定量的甲苯和KMnO4溶液置于图1装置中,在90℃时, 反应一段时间,再停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
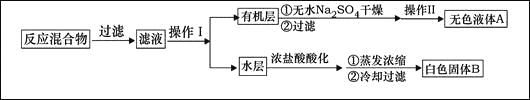
(1)无色液体A的结构简式为 。操作Ⅱspan>为 。
(2)如果滤液呈紫色,要先加亚硫酸氢钾,然后再加入浓盐酸酸化,加亚硫酸氢钾的目的是 。
(3)下列关于仪器的组装或者使用正确的是 。
A.抽滤可以加快过滤速度,得到较干燥的沉淀
B.安装电动搅拌器时,搅拌器下端不能与三颈烧瓶底、温度计等接触
C.图1回流搅拌装置应采用直接加热的方法
D.冷凝管中水的流向是下进上出
(4)除去残留在苯甲酸中的甲苯应先加入 ,分液,水层再加入 ,然后抽滤,干燥即可得到苯甲酸。
(5)纯度测定:称取1.220g产品,配成100mL溶液,取其中25.00mL溶液,进行滴定 ,消耗KOH物质的量为2.4×10-3mol。产品中苯甲酸质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com