
| A. | NaBiO3 | B. | Na4XeO6 | C. | K2S2O8 | D. | PbO2 |
分析 反应中氧化剂得电子,还原剂失电子,等量的还原剂与不同的氧化剂反应时,氧化剂中元素的化合价变化越大,反应消耗的氧化剂越少,据此分析.
解答 解:PbO2、NaBiO3、K2S2O8、Na4XeO6均可将Mn氧化为MnO4-,有关氧化剂则被还原为Pb2+、Bi3+、SO42-、Xe.若制得等物质的量的MnO4-,氧化剂中元素的化合价变化越大,反应消耗的氧化剂越少,PbO2的化合价变化2,NaBiO3的化合价变化3,K2S2O8的化合价变化2,Na4XeO6的化合价变化8,所以消耗的Na4XeO6最少;
故选B.
点评 本题考查了氧化还原反应,注意从化合价的角度分析,明确元素化合价的变化与得失电子数目的关系是解题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NaHSO4 | B. | Al2(SO4)3 | C. | NaOH | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Fe3+、SO42- | B. | Na+、[Al(OH)4]-、CO32- | ||
| C. | Na+、[Al(OH)4]-、SO42-、CO32- | D. | Na+、Ba2+、[Al(OH)4]- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 120℃,将wg甲醛在足量空气中燃烧,将生成产物用固体Na2O2(过量)吸收,固体增重wg | |
| B. | 24gMg带在足量CO2气体中燃烧,生成固体质量为40g | |
| C. | 相同物质的量的Al、Al2O3、Al(OH)3与足量NaOH溶液反应,溶液增重相等 | |
| D. | 在Fe3O4与足量浓硝酸的反应中,参加反应的Fe3O4与体现酸性的HNO3物质的量之比为1:10 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
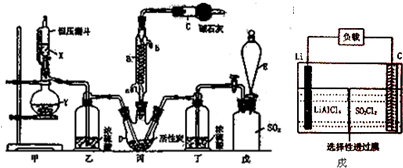
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com