
【题目】0.1 mol的镁、铝混合物溶于100 mL 2 moI/LH2SO4溶液中,然后再滴加l mol/LNaOH溶液。请回答:
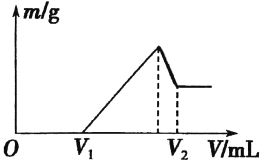
(l)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=160mL时,则金属粉末中n(Mg)=_________ mol,V2=________mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=________mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL2mol/L1硫酸溶解此混合物后,再加入450 mL l moI/LNaOH溶液,所得沉淀中无A1(OH)3。满足条件的a的取值范围是__________。
【答案】(1)0.06,440;(2)400;(3)![]()
【解析】
试题分析:(1)100mL 2molL-1的H2SO4溶液中硫酸的物质的量为0.1L×2mol/L=0.2mol,当V1=160mL时,此时,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,由Na+离子守恒可知,n(Na2SO4)=1/2n(Na+)=1/2n(NaOH)=0.5×0.16L×1mol/L=0.08mol。令MgSO4为xmol,Al2(SO4)3为ymol,则:根据Mg原子、Al原子守恒有:x+2y=0.1;根据SO42-离子守恒有:x+3y=0.2-0.08,联立方程,解得:x=0.06;y=0.02,所以金属粉末中n(Mg)=0.06mol,n(Al)=2y=2×0.02mol=0.04mol。滴加NaOH溶液到体积V2时,溶液是Na2SO4和NaAlO2混合液,根据SO42-离子、Na+离子和Al原子守恒有:n(NaOH) = 2n(Na2SO4)+n(NaAlO2) = 2n(H2SO4)+n(Al) = 2 × 0.2mol + 0.04mol = 0.44mol,所以,V2=0.44mol ÷ 1 mol/L=0.44L = 440mL;
(2)当溶液中Mg2+、Al3+恰好沉淀完全时,此时溶液是Na2SO4溶液,根据SO42-离子和Na+离子守恒有:n(Na+)=2n(Na2SO4)=2(H2SO4)=2×0.1L×2mol/L=0.4mol,所以V(NaOH)=0.4mol÷1mol/L=0.4L=400ml;
(3)由于为金属混合物,则a<1,Al的物质的量为0.1(1-a)mol,反应后的混合溶液,再加入450mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3,溶质为硫酸钠、偏铝酸钠,根据铝元素守恒可知n(NaAlO2)=0.1(1-a)mol,根据钠离子守恒,应满足n(NaOH) ≥ 2n(Na2SO4) + n(NaAlO2) ,即0.45 × 1 ≥ 2 × 0.1 × 2 + 0.1(1-a),解得a ≥ 0.5,故0.5 ≤ a < 1。


科目:高中化学 来源: 题型:
【题目】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.在250 mL容量瓶中配制250 mL烧碱溶液
B.用移液管(或碱式滴定管)量取25.00 mL 烧碱溶液于锥形瓶中并加几滴酚酞指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol·L-1的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
请完成下列问题:
(1)正确的操作步骤是(填写字母)__→__→__→D→__。
(2)操作D中液面应调整到_______________;
(3)以下操作会造成所测烧碱溶液浓度偏低的是( )
A.酸式滴定管未用待装溶液润洗
B.碱式滴定管未用待装溶液润洗
C.锥形瓶未用待装溶液润洗
D.在滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
(4)该烧碱样品的纯度计算式是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸二乙酯(D)可由石油气裂解得到的烯烃合成.回答下列问题:
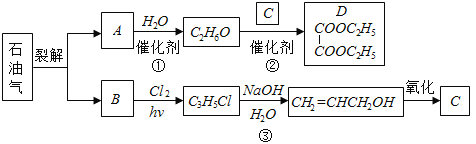
(1)B和A为同系物,B的结构简式为 .
(2)反应①的化学方程式为 ,其反应类型为 .
(3)反应③的反应类型为 .
(4)C的结构简式为 .
(5)反应②的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,是工业制硫酸的主要反应之一。
2SO3(g) ΔH<0,是工业制硫酸的主要反应之一。
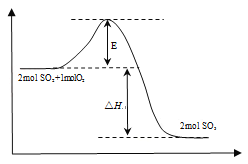
(1)该反应过程的能量变化如右图所示:E的大小对该反应的反应热有无影响_______(填“有”或“无”),该反应通常用V2O5作催化剂,加入V2O5后,改变的是图中的_______。
A.△H B.E C.△H – E D.△H + E
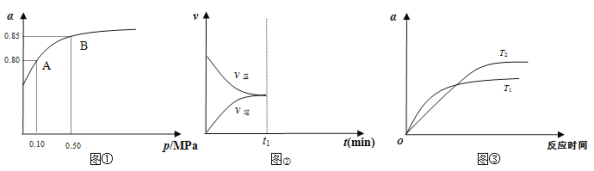
(2)某温度下,甲同学将2 mol SO2和1 mol O2置于密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图①所示,若A点二氧化硫的平衡浓度为0.04 mol/L,则容器的体积为_______L;图①中B点SO2、O2、SO3的平衡浓度之比为________________;反应到达平衡时,时间t1时缩小容器体积,请在图②中画出时间t1之后反应速率变化图像;图③为压强等于0.50 MPa时不同温度下SO2转化率与温度关系图,图中T2_____T1(填写“大于”或“小于”)
(3)在2 L的密闭容器中,乙同学投入2 mol SO2和b mol O2,25 min时达到平衡,如下图所示,在35 min时,改变某一条件,经过一段时间后,70 min时,反应再次达到平衡,回答下列问题:
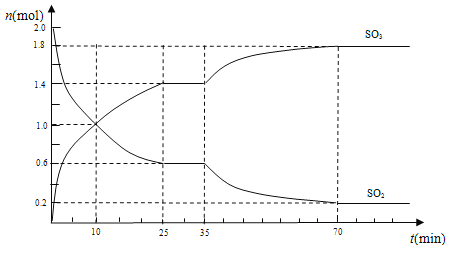
①10 min时,v(SO2)正________v(SO3)逆(填“>”“<”或“=”)
②求0~10 min时,v(O2)=______________
③反应开始至35 min时,测得反应共放热138.6 kJ,则反应2SO2(g)+O2(g)![]() 2SO3(g)△H=____kJ/mol
2SO3(g)△H=____kJ/mol
④35 min时,改变的条件可能是___________________
a.加入更多的V2O5
b.从容器中分离出少量O2
c.投入一定量的SO3
d.降低反应温度
e.往容器中加入N2,使容器压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏伽德罗常数的值。下列说法正确的是
A.标准状况下,22.4LCl2与足量的铁粉反应,转移的电子数为3NA
B.含23g钠元素的Na2O和Na2O2混合物中阴离子数目介于0.5NA和NA之间
C.在0℃、101kPa条件下,11.2L丁烷中含极性共价键数目为5NA
D.5NH4NO3![]() 4N2↑+2HNO3 +9H2O中氧化产物比还原产物每多14g,转移电子数为15NA
4N2↑+2HNO3 +9H2O中氧化产物比还原产物每多14g,转移电子数为15NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对有机物结构或性质的描述,错误的是
A. 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应
B. 乙二酸可与高锰酸钾溶液发生反应
C. 乙醇和乙烯的混合物1 mol,完全燃烧消耗 3 mol O2
D. 光照下, 2,2-二甲基丁烷与 Br2反应,其一溴取代物只有 2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com