
(1)白色的Fe(OH)2在空气中发生的颜色变化为
________________________;
(2)写出硅酸钠溶液在空气中变质的化学方程式:
____________________________;
(3)写出用熟石灰吸收氯气制漂白粉的化学方程式:
;
(4)将CaMg3Si4O12改写为氧化物的形式:[gkstk.Com]
__________________________________。[学优高考网gkstk]
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
室温时冰醋酸加水稀释过程中导电能力的变化如图所示。溶液的导电性体现了溶液中离子浓度大小。一般来说,溶液导电能力越强,离子浓度越大。
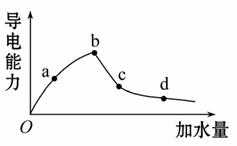
(1)图中O点[H+]=________mol·L-1。
(2)a、b、c、d四点中溶液的[H+]大小顺序为____________。电离程度大小顺序为______。电离平衡常数大小顺序为__________。(用“>”“=”或“<”来表示)
(3)若要使c点溶液中[CH3COO-]增大,而又不产生气体,则下列措施中可选择
_______ _。
_。
A.加水 B.加热
C.加锌粒 D.加固体NaOH
E.加很稀的 NaOH溶液 F.加固体CH3COON
NaOH溶液 F.加固体CH3COON a
a
(4)设d点醋酸溶液的浓度为c mol·L-1,此温度下醋酸的电离常数为Ka mol·L-1,达到平衡时醋酸分子浓度可近似为c mol·L-1,求平衡时溶液的pH(用Ka和c表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
甲醇脱水反应2CH3OH(g)===CH3OCH3(g)+H2O(g)
ΔH1=-23.9 kJ·mol-1
甲醇制烯烃反应2CH3OH(g)===C2H4(g)+2H2O(g) ΔH2=-29.1 kJ·mol-1
乙醇异构化反应C2H5OH(g)===CH3OCH3(g)
ΔH3=+50.7 kJ·mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)===C2H5OH(g)的ΔH=________ kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.Li在氧气中燃烧只生成Li2O[gkstk.Com]
B.将SO2通入过量BaCl2溶液可生成BaSO3沉淀
C.新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
D.将稀硫酸滴加到Fe(NO3)2溶液中无明显现象
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制480 mL含 NaClO 25%,密度为1.19 g/cm3的消毒液。下列说法正确的是 ( )
A.定容摇匀后,有少量溶液外流,则NaClO的物质的量浓度偏小
B.容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制
C.所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小
D.需要称量的NaClO固体的质量为142.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
在室温下的某密闭容中,将某气态烷烃与适量氧气混合,点火使之恰好完全燃烧后,冷却到室温,容器中压强为反应前压强的1/2,该气态烃是
A.甲烷 B.乙烷 C.丙烷 D. 丁烷
查看答案和解析>>
科目:高中化学 来源: 题型:
常见离子共存情况剖析
| 常见离子组合 | 共存情况 | 原因 |
| (1)Ba2+、Ca2+与SO | ||
| CO | ||
| (2)Mg2+与SO | ||
| (3)OH-与NH | ||
| (4)OH-与Mg2+、Al3+、Fe2+ | ||
| (5)H+与CH3COO-、ClO-、 | ||
| HCO | ||
| (6)Fe3+、Al3+与CO | ||
| HCO | ||
| (7)NO | ||
| (8)Fe3+与S2-、I- | ||
| (9)MnO | ||
| (10)NH |
查看答案和解析>>
科目:高中化学 来源: 题型:
在100 kPa和298 K时,有关反应的热化学方程式有:
H2(g)+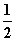 O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH1=-241.8 kJ·mol-1
H2(g)+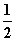 O2(g)===H2O(l) ΔH2=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH2=-285.8 kJ·mol-1
下列说法错误的是( )
A.H2燃烧生成1 mol H2O(g)时,放出241.8 kJ的热量
B.O2前面的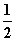 表示参加反应的O2的分子数目
表示参加反应的O2的分子数目
C.1mol物质完全燃烧生成稳定氧化物时放出的热量为燃烧热,H2的燃烧热为285.8 kJ·mol-1
D.1 mol液态水变成水蒸气时吸收44 kJ的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com