
10g含有杂质的 CaCO3和足量盐酸反应,产生了0.1mol CO2,杂质的组成可能是( )
A.KHCO3和MgCO3 B.K2CO3和Na2CO3
C.MgCO3和Na2CO3 D.Na2CO3和NaHCO3
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
10g含有杂质的CaCO3和足量的盐酸反应,产生CO20.1mol,则此样品中可能含有的杂质是( )
A.KHCO3和MgCO3 B.MgCO3和SiO2
C.K2CO3和SiO2 D.无法确定
查看答案和解析>>
科目:高中化学 来源:2011-2012学年广东省汕头市金山中学高一12月月考化学试卷 题型:实验题
(14分)某同学想通过利用下图所示装置(夹持装置略去)实验,探究SO2与Na2O2反应的产物
请分析:Ⅰ.装置B的作用 装置D的作用
Ⅱ.如何检验反应中是否有O2生成
Ⅲ.对C中固体产物提出如下假设:假设1:只有Na2SO3 假设2:只有Na2SO4
假设3:
(1)若按假设2进行,反应方程式为
(2)若Na2O2反应完全,为确定C中固体产物的成分,甲同学设计如下实验:
得出结论:假设2成立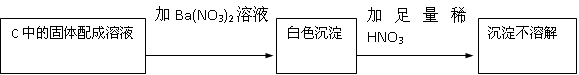
该方案是否合理 (填“是”或“否”),理由是
(3)若假设2成立,反应前后C管增加6.4g ,请计算10g含有杂质的Na2O2固体中,Na2O2的质量分数为 (所含的杂质不与SO2发生反应)
查看答案和解析>>
科目:高中化学 来源:新课标高一化学第一节无机非金属材料的主角-硅练习 题型:选择题
10g含有杂质的CaCO3和足量的盐酸反应,产生CO20.1mol,则此样品中可能含有的杂质是( )
A.KHCO3和MgCO3 B.MgCO3和SiO2
C.K2CO3和SiO2 D.无法确定
查看答案和解析>>
科目:高中化学 来源:2010年新疆乌鲁木齐一中高一上学期期末考试物理试卷 题型:选择题
10g含有杂质的CaCO3和足量的盐酸反应,产生CO20.1mol,则此样品中可能含有的杂质是( )
A.KHCO3和MgCO3 B.MgCO3和SiO2 C.K2CO3和SiO2 D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com