
【题目】在密闭容器中,反应X2(g)+Y2(g) ![]() 2XY(g);ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是 ( )
2XY(g);ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是 ( )
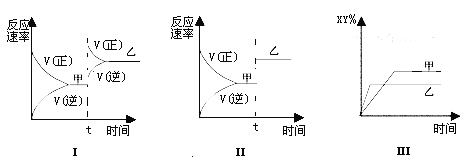
A. 图Ⅰ是加入适当催化剂的变化情况 B. 图Ⅱ是扩大容器体积的变化情况
C. 图Ⅲ是增大压强的变化情况 D. 图Ⅲ是升高温度的变化情况
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.苯酚沾在皮肤上用大量的水冲洗
B.氯乙烷与NaOH水溶液共热可制乙烯
C.为了鉴别己烯、甲苯和丙醛,可以使用新制Cu(OH)2悬浊液与溴水
D.CH3Cl可发生水解反应和消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图是化学实验中常用的几种装置。


请回答下列问题:
(1)指出有编号的仪器名称:①________________;②________________。
(2)利用上述A、B装置的组合可以制取的一种常见气体,写出实验室制取该气体的化学反应方程式:______________________________________。
(3)F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是____________________________,植物油上方原有的空气对实验的结果__________(填“有”或“没有”)明显影响。
(4)写出用石灰石和稀盐酸制取二氧化碳的化学方程式:___________________________________,可选用图中________和________(填标号)组装一套制取二氧化碳的装置。检验二氧化碳集满的方法是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氯化铜是重要的无机杀菌剂。
(1)碱式氯化铜有多种制备方法
①方法1: 45 ~ 50℃时,向CuCl悬浊液中持续通入空气得到Cu2 (OH)2 Cl2·3H2O, 该反应的化学方程式为_________________________。
②方法2: 先制得CuCl2,再与石灰乳反应生成碱式氯化铜。Cu与稀盐酸在持续通入空气的条件下反应生成CuCl2,Fe3+对该反应有催化作用,其催化原理如图所示。 M'的化学式为______。
(2)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O。 为测定某碱式氯化铜的组成, 进行下列实验:
①称取样品1.1160 g,用少量稀HNO3溶解后配成100.00 mL溶液A;
②取25. 00 mL溶液A,加入足量AgNO3溶液,得AgCl 0. 1722 g;③另取25. 00 mL溶液A,调节pH 4 ~ 5,用浓度为0.08000 mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++ H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液30.00 mL。通过计算确定该样品的化学式(写出计算过程)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程如下。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
下列说法错误的是( )
A. 在实验室实施操作①需要的玻璃仪器是漏斗、烧杯、玻璃棒
B. Mg(OH)2―→MgCl2的离子方程式为:Mg(OH)2+2H+===Mg2++2H2O
C. 操作②是将MgCl2溶液蒸干后冷却结晶
D. 操作④阴极和阳极产物的质量比是24∶71
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入lmol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1。
CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1。
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
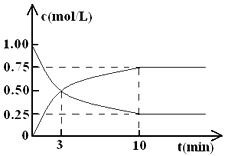
(1)从反应开始到平衡,氢气的平均反应速率v( H2 )= ________ ,CO2的转化率=________。
(2)该反应的平衡常数表达式k=__________ 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是_________________ (填编号)。
A.将H2O(g)从体系中分离B.充入He(g),使体系压强增大
C.升高温度 D.再充入lmolCO2和3molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 石油裂解是为了获得更多汽油,以满足迅速增长的汽车需要
B. 1mol冰醋酸和1mol乙醇反应生成的水分子数目为NA
C. 沸点:汽油<煤油<柴油<润滑油
D. 乙酸分子中不含醛基,所以不能与新制的Cu(OH)2悬浊液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z、M原子序数依次增大,元素W的一种核素的中子数为0,X的原子最外层电子数是次外层的2倍,Z与M同主族,Z2-电子层结构与氖原子相同。
(1)M在元素周期表中的位置是__________________________。
(2)化合物p由W、X、Y、M四种元素组成。已知向p溶液中加入FeCl3溶液,溶液变血红色;向p溶液中加入NaOH溶液并加热可放出使湿润的红色石蕊试纸变蓝的气体。p的化学式为_____________。
(3)由X、Y、Z三种元素可组成摩尔质量为84g·mol-1的物质q,且q分子中三种元素的原子个数之比为1:1:1。已知q分子中各原子均达到8电子稳定结构,且分子中不含双键,但含极性键和非极性键,q分子的结构式为_____________________。
(4)(XY)2的性质与Cl2相似,(XY)2与NaOH溶液常温下反应的离子方程式为________。
(5)常温下,1molZ3能与Y的最简单氢化物反应,生成一种常见的盐和1molZ2,该反应的化学方程式为____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com