
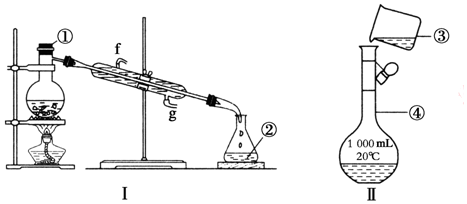
分析 (1)由图可知仪器的名称;
(2)具有塞子或活塞的仪器使用前需要检验是否漏水;
(3)装置I分离四氯化碳和酒精的混合物,为蒸馏原理,需要温度计测定馏分的温度,且冷却水下进上出,冷却效果好;
(4)配制0.1mol/LNaOH溶液450mL,选500mL容量瓶,且转移液体需要玻璃棒引流.
解答 解:(1)由图可知仪器①②③的名称分别为蒸馏烧瓶、锥形瓶、1000mL容量瓶,故答案为:蒸馏烧瓶;锥形瓶;1000mL容量瓶;
(2)具仪器①~④中,使用前必须检查是否漏水的有④,故答案为:④;
(3)装置I分离四氯化碳和酒精的混合物,为蒸馏原理,图中缺少酒精灯,需要温度计测定馏分的温度,冷凝管的进水口是g,
故答案为:酒精灯;蒸馏;g;
(4)配制0.1mol/LNaOH溶液450mL,选500mL容量瓶,且转移液体需要玻璃棒引流,则图中错误为容量瓶规格错误、缺少玻璃棒引流,
故答案为:容量瓶规格错误;缺少玻璃棒引流.
点评 本题考查混合物分离提纯,为高频考点,把握实验装置的作用、仪器的使用、混合物分离提纯为解答本题关键,侧重分析与实验能力的考查,注意容量瓶具有固定的规格,题目难度不大.


 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 戊烷的分子式 C5H8 | B. | 质量数为37的氯原子${\;}_{37}^{17}$Cl | ||
| C. | 乙烯的结构简式 C2H4 | D. | Cl-的结构示意图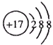 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若管道漏气遇氨就会产生白烟 | |
| B. | 生成1 mol N2有3 mol电子转移 | |
| C. | 发生氧化反应与还原反应的分子个数比是2:3 | |
| D. | 该反应利用了Cl2的强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
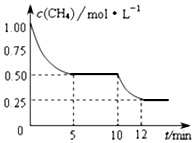 在1L密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.
在1L密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×l0-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | NaHCO3溶液中,c(Na+)>c(HCO3-)>c(H2CO3)>c(OH-) | |
| B. | 将amol•L-1HCN溶液与amol•L-1NaOH溶液等体积混合后,测得所得溶液显碱性,则c(CN-)>c(Na+) | |
| C. | 等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) | |
| D. | 1.0 mol•L-1Na2CO3溶液:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当2a=b时,溶液中生成的沉淀质量最大 | |
| B. | 当a=2b时,发生的离子反应为2NH4++SO42-+Ba2++2OH-═BaSO4↓+2NH3•H2O | |
| C. | 当2b≤3a时,发生的离子反应为3SO42-+2Al3++3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ | |
| D. | 当2a<b≤2.5a时,溶液中的n(AlO2-)为0.02(b-2a) mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com