
| A. |  石油的分馏 | B. | 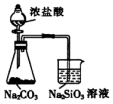 验证碳酸的酸性强于硅酸 | ||
| C. |  组装原电池 | D. |  乙酸乙酯的制备 |
分析 A.分馏时温度计测定馏分的温度;
B.浓盐酸易挥发,盐酸与硅酸钠反应;
C.没有构成闭合回路;
D.乙酸与乙醇在浓硫酸作用下发生酯化反应,饱和碳酸钠可吸收乙醇、除去乙酸、降低酯的溶解度.
解答 解:A.分馏时温度计测定馏分的温度,则温度计的水银球应在烧瓶的支管口出,故A错误;
B.浓盐酸易挥发,盐酸与硅酸钠反应,则不能比较碳酸、硅酸的酸性,故B错误;
C.没有构成闭合回路,不能形成原电池,故C错误;
D.乙酸与乙醇在浓硫酸作用下发生酯化反应,饱和碳酸钠可吸收乙醇、除去乙酸、降低酯的溶解度,且图中导管在液面上,可防止倒吸,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、混合物分离提纯、原电池、有机物制备实验为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 增大压强可加快该反应速率 | |
| B. | 加入合适的催化剂可改变该反应的反应热 | |
| C. | 达到平衡时,用任意组分表示正逆反应速率都有v(正)=v(逆) | |
| D. | 达到平衡时,H2O2转化率为100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 导线中电流方向:锌→铜 | B. | Zn为正极,Cu为负极 | ||
| C. | 溶液中H+向锌片移动 | D. | 该装置能将化学能转变为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe位于元素周期表第四周期,VⅢA族 | |
| B. | K在同周期中,原子半径最大,金属性最强 | |
| C. | .高铁酸钾具有强氧化性 | |
| D. | 高铁酸钾中Fe的化合价为+6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的球棍模型: | B. | NH4Br的电子式: | ||
| C. | 2,2-二甲基丙烷的结构简式: | D. | 乙烯的实验式为CH2=CH2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com