
| ŃōĄė×Ó | K+”¢Mg2”¢Fe3+”¢Al3+ |
| ŅõĄė×Ó | 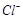 ”¢ ”¢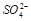 ”¢ ”¢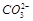 |
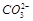 £©="0.2" mol/L B£®C(K+)Ņ»¶ØĪŖ0.6mol/L
£©="0.2" mol/L B£®C(K+)Ņ»¶ØĪŖ0.6mol/L 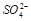 ŗĶ
ŗĶ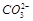
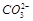 £©="0.02mol”Ā0.1L=0.2" mol/L”£¶ųƻӊȷ¶ØŹĒ·ńÓŠĀČĄė×Ó£¬ĖłŅŌB”¢DŃ”Ļī¶¼“ķ£¬Ń”ŌńC”£
£©="0.02mol”Ā0.1L=0.2" mol/L”£¶ųƻӊȷ¶ØŹĒ·ńÓŠĀČĄė×Ó£¬ĖłŅŌB”¢DŃ”Ļī¶¼“ķ£¬Ń”ŌńC”£


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®NH4+ | B£®H+ | C£®NO3£ | D£®H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

| A£®ĻņNaAlO2ČÜŅŗÖŠµĪČėHClÖĮ¹żĮæ |
| B£®Ļņ³ĪĒåŹÆ»ŅĖ®ÖŠĶØČėCO2ÖĮ¹żĮæ |
| C£®Ļņŗ¬ÓŠŃĪĖįµÄAlCl3ČÜŅŗÖŠµĪČėNaOHČÜŅŗÖĮ¹żĮæ |
| D£®Ļņŗ¬ÓŠµČĪļÖŹµÄĮæµÄCa(OH)2”¢KOHµÄ»ģŗĻČÜŅŗÖŠĶØČėCO2ÖĮ³ĮµķĻūŹ§ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ŌŚpH=1µÄČÜŅŗÖŠ£¬Cu2+”¢Fe2+”¢NO3-ŗĶSO42-ÄÜ“óĮæ¹²“ę |
| B£®ÓƶčŠŌµē¼«µē½ā±„ŗĶĀČ»ÆÄĘČÜŅŗµÄĄė×Ó·½³ĢŹ½£ŗ2Cl- + 2H+ = H2”ü+ Cl2”ü |
| C£®Ć¾ĀĮŗĻ½š±»¼īŅŗøÆŹ“Ź±£¬øŗ¼«·“Ó¦Ź½ĪŖ£ŗMg ”Ŗ 2e£ = Mg2£« |
| D£®¼ģŃéijĪ“ÖŖČÜŅŗÖŠŹĒ·ńŗ¬SO42£Ź±£¬Ó¦ĻČ¼ÓŃĪĖįĖį»Æ£¬ŌŁ¼ÓBaCl2ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®H2SO4 | B£®KOH | C£®BaCl2 | D£®Na2CO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
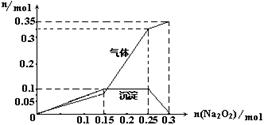
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ÓĆCO»¹ŌŃõ»ÆĢśĄ“Į¶Ģś | B£®ÓĆŠæŗĶĻ”ŃĪĖį·“Ó¦ÖĘĒāĘų |
| C£®ÓĆĻ”ĮņĖį³żĢśŠā | D£®CO2ĶØČė³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| ŃōĄė×Ó | Na+ Mg2+ Fe2+ Al3+ Fe3+ |
| ŅõĄė×Ó | OH- Cl- CO32- NO3- SO42- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com