
【题目】美国药物学家最近合成种可治疗高血压的有机物K,其合成路线如图所示。

已知:①A的核磁共振氢谱中只有1组峰;
②G和H按物质的量之比1:3反应生成I;
③R1CHO+R2CH2CHO 。
。
(1)A的名称为____________ (用系统命名法命名),由B生成C的反应类型为_______。
(2)写出D的结构简式:______________。
(3)G和H反应生成I的化学方程式为:______________。
(4)E有多种同分异构体,其中既能发生银镜反应又能发生水解反应的有__________种(不考虑立体异构)。
(5)参照上述合成路线,设计一条以G为原料制备1,3-丁二烯CH2=CH-CH=CH2的合成路线_______。
【答案】 2,2-二甲基丙烷 取代反应(或水解反应) 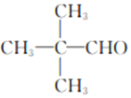 CH3CHO+3HCHO
CH3CHO+3HCHO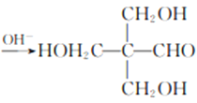 4
4 ![]()
【解析】已知A的核磁共振氢谱中只有1组峰,根据A的分子式可知A是新戊烷。A与氯气发生取代反应生成B是(CH3)3CCH2Cl,B水解生成C是(CH3)3CCH2OH,C发生催化氧化生成D是(CH3)3CCHO,D继续氧化生成E是(CH3)3CCOOH。葡萄糖在酒化酶的作用下生成F是乙醇,F发生催化氧化生成G是乙醛,根据已知信息②③可知乙醛和甲醛发生反应生成I,I与氢气发生加成反应生成J为C(CH2OH)4。E与J发生酯化反应生成K。据此解答。
(1)A是新戊烷,其系统命名法的名称为2,2-二甲基丙烷;由B生成C是卤代烃的水解,其反应类型为取代反应(或水解反应)。
(2)D的结构简式为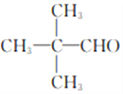 。
。
(3)G和H反应生成I的化学方程式为CH3CHO+3HCHO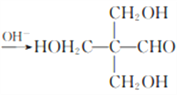 。
。
(4)E有多种同分异构体,其中既能发生银镜反应又能发生水解反应,说明是甲酸和丁醇形成的酯基,丁醇有4种,所以符合条件的有机物同分异构体有4种。
(5)根据逆推法结合已知信息可知以G为原料制备1,3-丁二烯的合成路线为![]() 。
。


科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )
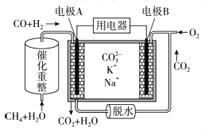
A. 反应CH4+H2O==3H2+CO,每消耗11.2L CH4转移3mol电子
B. 电极B上发生的电极反应为O2+2CO2+4e-==2CO32-
C. 电池工作时,电子通过熔融盐由电极B向电极A移动
D. 电极A上CO参与的电极反应为CO+4OH- —2e- == CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下为无色液体,而且密度大于水的是
①苯 ②硝基苯 ③溴苯 ④四氯化碳 ⑤溴乙烷 ⑥乙酸乙酯
A. ②③④⑤B. ③④⑤⑥C. ①⑥D. ②③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中的主要污染物是 NO、NO2 和 CO。处理汽车尾气,可实现绿色环保、节能减排。
(1)用 NaOH 溶液吸收 NO、NO2,当 n(NO)∶n(NO2)=1 时只生成一种盐,该盐的化学式为 _________ 。
(2)已知:①CO 的燃烧热△H1=-282 kJ·mol-1;
②N2(g)+O2(g)=2NO(g)△H2=+183 kJ·mol1。
写出 NO 和 CO 反应生成无污染性气体的热化学反应方程式______________________。
(3)在密闭容器中充入 10molCO 和 8molNO,发生反应,如图为平衡时 NO 的体积分数与温度,压强的关系。
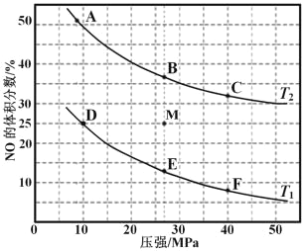
①若反应在恒容密闭容器中进行,下列图像正确且能说明反应达到平衡状态的是_____。
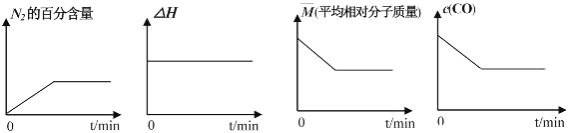
A B C D
②该反应达到平衡后,为在提高反应速率的同时提高 NO 的转化率,可采取的措施有_____(填字母)。
A.升高温度 B.缩小容器的体积
C.增加 CO 的浓度 D.改用高效催化剂
③在压强为 10MPa、温度为 T1 条件下,若反应进行到 20 min 达到平衡状态,容器的体积为 4 L,则此时 NO 的转化率=________________ ,用 N2 的浓度变化表示的平均反应速率 v(N2)= _______________,该温度下平衡常数 Kp=___________________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;保留两位有效数字)。
④若在 M 点对反应容器降温,同时缩小体积至体系压强增大,重新达到的化学平衡状态可能是图中 A~F 点中的_____点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题:

(1)②表示的元素是 ______ (填元素符号)。
(2)①与⑤两种元素相比较,原子半径较大的是 ______ (填元素符号),其非金属性较强的是 ______ (填元素符号),其最高正价氧化物水化物酸性较强的酸是 ______ (填分子式)。
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是 ______ (填化学式)。③与⑥两种元素所形成化合物的电子式是 ______ 。
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式: ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于消去反应的是( )
①CH3CH2OH+HBr![]() CH3CH2Br+H2O
CH3CH2Br+H2O
②2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
③CH3CH2CH2Br![]() CH3CH===CH2↑+HBr
CH3CH===CH2↑+HBr
④2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
⑤CH3CH2Br+NaOH ![]() CH3CH2OH+NaBr
CH3CH2OH+NaBr
⑥![]()
⑦CH3CH2OH![]() CH2===CH2↑+H2O
CH2===CH2↑+H2O
⑧CH3CH2OH+HCOOH![]() HCOOCH2CH3+H2O
HCOOCH2CH3+H2O
A. ⑤⑦⑧ B. ②③ C. ③④⑤ D. ③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的位置如下图所示,若W原子最外层电子数是其内层电子总数的3/5。下列说法中,正确的是
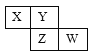
A. X只有一种氧化物
B. 气态氢化物的稳定性Z>W
C. 原子半径由大到小排列顺序Z>Y>X
D. 元素X是自然界中形成化合物种类最多的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在空气中,钢铁与食盐水接触,发生吸氧腐蚀,在负极上发生的电极反应是( )
A. Fe-2e-=Fe2+B. 2H++2e-=H2↑
C. Na++e-=NaD. 2H2O+O2+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】比较过氧化氢在四种不同条件下发生分解反应:2H2O2=2H2O+O2↑,其中产生O2的反应速率最大的试验编号是( )
实验编号 | 温度 | 过氧化氢的质量分数 | 催化剂 |
A | 20℃ | 4% | 无 |
B | 50℃ | 4% | 有 |
C | 20℃ | 12% | 无 |
D | 50℃ | 12% | 有 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com