
【题目】芳香族化合物A的分子式为C7H6O2,将它与NaHCO3溶液混合加热,有酸性气体产生.那么包括A在内,属于芳香族化合物的A的同分异构体的数目是
A. 5 B. 4 C. 3 D. 2
科目:高中化学 来源: 题型:
【题目】某溶液中含有NH4+、Na+、Mg2+、NO3-4种离子,若向其中加入少量过氧化钠固体后溶液中离子浓度基本保持不变的是( )
A. Mg2+B. Na+C. NH4+D. NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 浓盐酸、浓硫酸、浓硝酸均属于强电解质
B. SiO2、SO2、SO3均属于酸性氧化物
C. 纯碱的分子式是Na2CO3
D. 根据是否具有丁达尔效应,将分散系分为溶液、胶体和浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Sn(核电荷数为50)是人类最早使用的元素之一,能形成SnCl2,SnCl4两种氯化物,SnCl2常温下为白色晶体,具有一维链状的聚合结构,气态时以单分子形式存在,而SnCl4常温下为无色液体.白锡和灰锡是Sn的两种同素异形体,白锡的晶体结构中Sn原子的配位数为4和6,灰锡的晶体结构与金刚石的晶体结构相似.白锡的密度大于灰锡的密度.

(1)Sn元素外围电子排布式为______.
(2)SnCl2的一维链状聚合结构如图1所示,在分子结构中存在的化学键是______.
(3)SnCl4与CCl4中沸点较高的是______.原因是______.
(4)锡的某种氧化物的晶胞如图2,其化学式为______.
(5)解释白锡分子的密度大于灰锡的密度的原因____________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“春蚕到死丝方尽,蜡炬成灰泪始干”是唐代诗人李商隐的著名诗句,下列关于该诗句中所涉及物质的说法错误的是( )
A. 蚕丝的主要成分是蛋白质B. “蜡炬成灰”过程中发生了氧化反应
C. 蚕丝属于天然高分子材料D. 古代的蜡是高级脂肪酸酯,属于高分子聚合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以以乙炔为原料,通过下图所示步骤能合成一种高分子涤纶G(转化过程中的部分反应条件及部分产物已略去):

其中A、B、C、D分别代表一种有机物,B分子中无甲基。
已知:-C≡CH+ 
![]()


请回答下列问题:
(1)A→B的化学反应类型是______。
写出B→C的化学反应方程式:____________。
(2)E 和H2完全加成得到的物质的结构简式是____________。
(3)写出符合下列条件的E的同分异构体________。
①含有苯环 ②属于酯类 ③可发生银镜反应 ④苯环上有两种不同环境的H。
(4)下列说法正确的是______(填字母代号)。
A.上述流程中,乙炔、有机物B、有机物E都可发生聚合反应
B.有机物E能使酸性KMnO4溶液褪色,可说明E含碳碳双键
C.有机物C的名称为丁二醛,具有还原性
D. 35%~40%的甲醛(HCHO)溶液俗称福尔马林溶液,能使蛋白质变性
(5)天然纤维的吸湿性优于合成纤维,下列合成纤维中吸湿性较好的是____(填字母代号)。
A.聚酰胺纤维(锦纶) B.聚酯纤维(涤纶)
C.聚乙烯醇缩甲醛纤维(维纶) D.聚丙烯纤维(丙纶)
(6)请写出F生成G的化学反应方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物广泛存在于自然界。请回答下列问题:
(1)以CO2与NH3为原料可合成尿素[CO(NH2)2]。已知:
①2NH3(g) + CO2(g) === NH2COONH4(s) △H=-159.47 kJ·mol-1
②NH2COONH4(s) === CO(NH2)2(s) + H2O(g) △H=+116.49 kJ·mol-1
③H2O(l) === H2O(g) △H=+88.0 kJ·mol-1
写出NH3和CO2合成尿素和液态水的热化学方程式_____________。
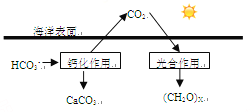
(2)海洋是地球上碳元素的最大“吸收池”。
①溶于海水中的CO2主要以四种无机碳形式存在,即:CO2、H2CO3、___________、_________。
②在海洋碳循环中,可通过右图所示的途径固碳。写出钙化作用的离子方程式_____________。
(3)常温常压下,空气中的CO2溶于水中达到平衡时,其转化关系如下:
①CO2 + H2O![]() H2CO3 K=1.8×10-3
H2CO3 K=1.8×10-3
②H2CO3![]() H++HCO3- K a 1=4.3×10-7,
H++HCO3- K a 1=4.3×10-7,
③HCO3-![]() H++CO32- K a2=5.6×10-11,
H++CO32- K a2=5.6×10-11,
通常情况下,海水的pH约为8,若忽略水的电离及H2CO3的第二级电离,则溶液中c(CO2)=____ mol/L。(保留两位有效数字)
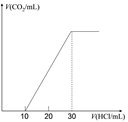
(4)为了测量某湖水中无机碳含量,量取100mL湖水,酸化后用 N2吹出CO2,再用NaOH溶液吸收。用1.0mol/L盐酸滴定吸收液,生成的V(CO2)随V(盐酸) 变化关系如左图所示,则吸收液中离子浓度由大到小的顺序为______,湖水中无机碳的浓度为___mol/L。
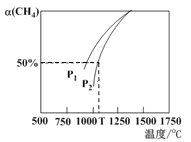
(5)用CO2和天然气可以制备CO和H2,CO2(g) +CH4(g) ![]() 2CO(g)+2H2(g)。密闭容器中浓度均为0. 1 mol/L的CH4与CO2,在一定条件下反应,测得CH4 的平衡转化率与温度及压强的关系如右图所示,则压强P1 ____P2(填“>”或“<”)。若P2= 3MPa,则T°C时该反应的平衡常数 Kp =_____MPa2
2CO(g)+2H2(g)。密闭容器中浓度均为0. 1 mol/L的CH4与CO2,在一定条件下反应,测得CH4 的平衡转化率与温度及压强的关系如右图所示,则压强P1 ____P2(填“>”或“<”)。若P2= 3MPa,则T°C时该反应的平衡常数 Kp =_____MPa2
(用平衡分压代替平衡浓度计算, 分压=总压×物质的量分数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com