
| A. | ④⑥ | B. | ②④⑥ | C. | 仅有⑥ | D. | ①③ |
分析 ①偏铝酸钠溶液与少量盐酸:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl;偏铝酸钠溶液与过量盐酸:NaAlO2+4HCl=AlCl3+2H2O↑;
②碳酸钠与少量盐酸:Na2CO3+HCl=NaHCO3+NaCl;与过量盐酸反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
③氨水少量生成沉淀,氨水过量沉淀溶解;
④苯酚钠溶液与二氧化碳反应无论二氧化碳过量还是不足,都只反应生成苯酚和碳酸氢钠;
⑤酸式盐和对应碱的反应,前者过量,生成的碳酸根离子过量,后者过量,氢氧根离子过量;
⑥硫酸铝溶液与氨水:Al2(SO4)3+6NH3.H2O=2Al(OH)3↓+3(NH4)2SO4;
解答 解:①偏铝酸钠溶液与少量盐酸:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl;偏铝酸钠溶液与过量盐酸:NaAlO2+4HCl=AlCl3+2H2O↑,偏铝酸钠溶液与盐酸,反应物用量不同,发生反应不同,离子方程式不同,故①不选;
②碳酸钠与少量盐酸:Na2CO3+HCl=NaHCO3+NaCl;与过量盐酸反应:Na2CO3+2HCl=2NaCl+H2O+CO2↑,反应物用量不同,发生反应不同,离子方程式不同,故②不选;
③硝酸银中滴氨水是银氨溶液的配制,先产生白色氢氧化银沉淀,继续滴加,形成配合物银氨络离子(银氨溶液)使沉淀溶解.先发生:Ag ++NH3•H2O=AgOH↓+NH4+,后发生:AgOH+2NH3•H2O=[Ag(NH3)2]++OH-+2H2O;氨水中滴硝酸银,一开始就产生银氨溶液(氨水过量),量不同,生成产物不同,故③不选;
④苯酚钠中通入二氧化碳反应生成碳酸氢钠和苯酚,与量无关,C6H5O-+CO2+H2O→C6H5OH+HCO3-,故④选;
⑤碳酸氢钠溶液与澄清石灰水的反应:前者过量,2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O,后者过量,HCO3-+Ca2++OH-=CaCO3↓+H2O,量不同,生成产物不同,故⑤不选;
⑥硫酸铝溶液与氨水:Al2(SO4)3+6NH3.H2O=2Al(OH)3↓+3(NH4)2SO4,反应产物与反应物用量无关,故⑥选;
故选:A.
点评 本题考查离子反应,为高频考点,把握发生的反应及离子反应中量对反应的影响为解答的关键,侧重与量有关的离子反应考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
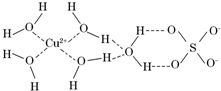 第四周期的许多金属能形成配合物.科学家通过X射线测得胆矾结构示意图可简单表示如下:
第四周期的许多金属能形成配合物.科学家通过X射线测得胆矾结构示意图可简单表示如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在共价化合物中一定含有共价键 | |
| B. | 由非金属元素组成的化合物一定是共价化合物 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 双原子单质分子中的共价键一定是非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
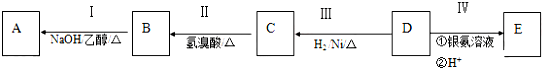
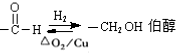

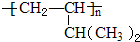
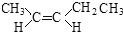
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②③⑤ | C. | ①②④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
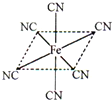 铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如图;已知CN-与N2结构相似,1molCN-中π键数目为2NA.
铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如图;已知CN-与N2结构相似,1molCN-中π键数目为2NA.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
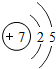 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元 素 | Mn | Fe | |
| 电离能 /kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
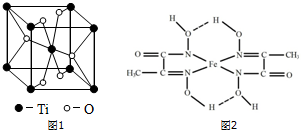
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com