
【题目】碳热还原法广泛用于合金及材料的制备。回答下列问题:
(1)一种制备氮氧化铝的反应原理为23Al2O3+15C+5N2=2Al23O27N5+15CO ,产物Al23O27N5中氮的化合价为______,该反应中每生成1 mol Al23O27N5,转移的电子数为________NA。
(2)真空碳热冶铝法包含很多反应,其中的三个反应如下:
Ⅰ.Al2O3(s)+3C(s)=Al2OC(s)+2CO(g) ΔH1
Ⅱ.2Al2OC(s)+3C(s)=Al4C3(s)+2CO(g) ΔH2
Ⅲ.2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g) ΔH3
①ΔH3=_________(用ΔH1、ΔH2表示)。
②Al4C3可与足量盐酸反应制备一种烃。该反应的化学方程式为________________。
(3)下列是碳热还原法制锰合金的三个反应,CO与CO2平衡分压比的自然对数值与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数)。
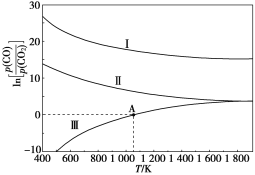
Ⅰ.Mn3C(s)+4CO2(g)![]() 3MnO(s)+5CO(g) Kp(Ⅰ)
3MnO(s)+5CO(g) Kp(Ⅰ)
Ⅱ.Mn(s)+CO2(g)![]() MnO(s)+CO(g) Kp(Ⅱ)
MnO(s)+CO(g) Kp(Ⅱ)
Ⅲ.Mn3C(s)+CO2(g)![]() 3Mn(s)+2CO(g) Kp(Ⅲ)
3Mn(s)+2CO(g) Kp(Ⅲ)
①ΔH>0的反应是____(填“Ⅰ”“Ⅱ”或“Ⅲ”)。
②1 200 K时,在一体积为2 L的恒容密闭容器中有17.7 g Mn3C(s)和0.4 mol CO2,只发生反应Ⅰ,5 min 后达到平衡,此时CO的浓度为0.125 mol/L,则0~5 min内v(CO2)=_________。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应Ⅱ达到平衡的是____(填字母)。
A.容器的体积不再改变 B.固体的质量不再改变 C.气体的总质量不再改变
【答案】-3 15 2ΔH1+ΔH2 Al4C3+12HCl=4AlCl3+3CH4↑ Ⅲ 0.02 mol·L-1·min-1 BC
【解析】
(1)化合价通过物质化合价代数和为0计算可得;转移电子数通过氧化反应得失电子守恒计算可知;
(2)通过盖斯定律计算ΔH3;Al4C3可与足量盐酸反应制取烃类C前后化合价不变可知烃为CH4;
(3)由图中信息可知,反应Ⅲ升高温度,ln K增大,则K增大,平衡正向移动,正反应为吸热反应;反应![]() 为气体体积不变的放热反应,根据“变量不变达平衡”进行判断。
为气体体积不变的放热反应,根据“变量不变达平衡”进行判断。
(1)Al23O27N5中Al为+3价,O为-2价,设氮的化合价为x,则(+3)×23+(-2)×27+5x=0,解得x=-3,反应![]() 中N的化合价降低3价,则每生成1 mol Al23O27N5,转移的电子数为5×3NA=15NA。
中N的化合价降低3价,则每生成1 mol Al23O27N5,转移的电子数为5×3NA=15NA。
故答案为:-3;15;
(2)已知Ⅰ![]() ΔH1;Ⅱ.
ΔH1;Ⅱ.![]() ΔH2;Ⅲ.
ΔH2;Ⅲ.![]() ΔH3;①根据盖斯定律,由Ⅰ×2+Ⅱ得反应Ⅲ
ΔH3;①根据盖斯定律,由Ⅰ×2+Ⅱ得反应Ⅲ![]() ΔH3=2ΔH1+ΔH2;②Al4C3可与足量盐酸反应制备一种最简单的烃CH4,根据质量守恒配平可得反应的化学方程式为
ΔH3=2ΔH1+ΔH2;②Al4C3可与足量盐酸反应制备一种最简单的烃CH4,根据质量守恒配平可得反应的化学方程式为![]() 。
。
故答案为:2ΔH1+ΔH2;![]() ;
;
(3)①由图中信息可知,反应Ⅲ升高温度,ln K增大,则K增大,平衡正向移动,正反应为吸热反应,ΔH>0,故选Ⅲ;
②0~5 min内v(CO2)=![]() v(CO)=
v(CO)=![]() ×
×![]() =0.02 mol·L-1·min-1;
=0.02 mol·L-1·min-1;
③反应Ⅱ.![]() 为气体体积不变的放热反应,根据“变量不变达平衡”进行判断:
为气体体积不变的放热反应,根据“变量不变达平衡”进行判断:
A.反应为气体不变的反应,反应过程容器的体积不是变量,不能作为平衡状态的判断依据;
B.反应是一个固体质量增大的反应,固体的质量为变量,当固体的质量不再改变说明达到平衡状态;
C.反应是一个气体质量减小的反应,气体的总质量为变量,当不再改变说明达平衡状态。
故答案为:Ⅲ;0.02 mol·L-1·min-1;BC。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氮的化合物应用广泛,但氮氧化物是重要的空气污染物,应降低其排放。
(1)用CO2和NH3可合成氮肥尿素
已知:①2NH3(g)+CO2(g)===NH2CO2NH4(s) △H=-159.5kJ·mol-1
②NH2CO2NH4(s)===CO(NH2)2(s)+H2O(g) △H=+116.5kJ·mol-1
③H2O(1)===H2O(g) △H=+44kJ·mol-1
用CO2和NH3合成尿素(副产物是液态水)的热化学方程式为___________。
(2)工业上常用如下反应消除氮氧化物的污染:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H
N2(g)+CO2(g)+2H2O(g) △H
在温度为T1和T2时,分别将0.40 mol CH4和1.0 mol NO2充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如图所示:
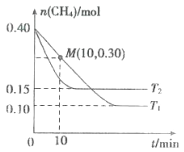
①根据如图判断该反应的△H___________0(填“>”“<”或“=”),理由是___________。
②温度为T1时,0~10min内NO2的平均反应速率v(NO)2=___________,反应的平衡常数K=______(保留三位小数)
③该反应达到平衡后,为再提高反应速率同时提高NO2的转化率,可采取的措施有______(填编号)。
A.改用高效催化剂 B.升高温度
C.缩小容器的体积 D.增加CH4的浓度
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3===7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH___________(填“增大”“减小”或“不变”),负极的电极反应式为___________。
(4)氮的一种氢化物HN3,其水溶液酸性与醋酸相似,则NaN3溶液中各离子浓度由大到小的顺序为___________;常温下将 a mol·L-1的HN3与b mol·L-1的Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N3-),则该混合物溶液呈___________(填“酸”“碱”或“中”)性,溶液中c(HN3)=___________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3BrF3+5H2O===HBrO3+Br2+9HF+O2↑中,若有5 mol H2O作为还原剂时,被还原的BrF3的物质的量为( )
A. 3 mol B. 2 mol C. ![]() mol D.
mol D. ![]() mol
mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有室温下溶质浓度均为![]() 的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
(1)在④溶液中,各离子浓度大小顺序为:____________
(2)将③、⑥混合后,若溶液呈现中性,则消耗量溶液的体积为③____________⑥(填“>”、“=”或“<”),溶液中的离子浓度由大到小的顺序为____________
(3)在常温下,将100mL的②与100mL的⑥溶液混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=____________(已知![]() )
)
(4)在常温下,六种液体的pH由大到小的顺序是____________
(5)若将③溶液和⑥溶液按体积比2:1混合后溶液呈酸性,则混合后溶液中![]() __________
__________![]() (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
(6)常温下将③溶液加水稀释过程中,下列表达式的数据一定变大的是______
A、![]() B、
B、![]() C、
C、![]() D、
D、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 乙烷和新戊烷分子中所含甲基数之比为1∶1
B. 甲苯能发生加成反应、氧化反应和取代反应
C. 聚乙烯能使酸性KMnO4溶液和溴水褪色,但二者原理不同
D. ![]() 和C4H10的二氯代物的数目相同(不含立体异构)
和C4H10的二氯代物的数目相同(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Fe和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下,其中正确的是( )
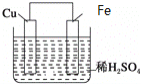
①Fe为正极,Cu为负极;②H+向铁电极移动;③电子是由Fe经外电路流向Cu;④内电路电流由铁电极流向铜电极;⑤若有1mol电子流过导线,则产生的![]() 为
为![]() ;⑥负极的电极反应式为
;⑥负极的电极反应式为![]() 。
。
A.③④B.③⑤C.③④⑤D.③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化合物X(结构如图)的叙述正确的是( )
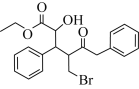
A.X分子存在2个手性碳原子
B.X分子能发生氧化、取代、消去反应
C.X分子中所有碳原子可能在同一平面上
D.1molX与足量NaOH溶液反应,最多消耗2molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中处处有化学,下列有关说法正确的是( )
A.草木灰与铵态氮肥不能混合施用与盐类水解有关
B.焊接时用NH4Cl溶液除锈与盐类水解无关
C.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂
D.生活中Cl2和NaOH制取消毒液,运用了盐类的水解原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C和CuO在高温下反应可能生成Cu、![]() 、
、![]() 、CO。现将
、CO。现将![]() 碳粉跟
碳粉跟![]() 混合,在硬质试管中隔绝空气高温加热,将生成的气体全部通入足量NaOH溶液中,并收集残余的气体,测得溶液增加的质量为
混合,在硬质试管中隔绝空气高温加热,将生成的气体全部通入足量NaOH溶液中,并收集残余的气体,测得溶液增加的质量为![]() ,残余气体在标准状况下的体积为
,残余气体在标准状况下的体积为![]() 。下列说法不正确的是
。下列说法不正确的是
A.在硬质试管中隔绝空气高温加热固体混合物时,有![]() 碳参加了反应
碳参加了反应
B.试管中发生的所有氧化还原反应共转移电子![]()
C.反应后试管中剩余的固体混合物的总质量为![]()
D.反应生成铜和氧化亚铜的总物质的量为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com