
【题目】某溶液中含有VO2+和Cr2O72-,现向此溶液中滴入29.00mL0.1mol/L的FeSO4溶液,恰好使VO2+→VO2+,Cr2O72-→Cr3+。再滴入2.00mL,0.020mol/LKMnO4溶液,又恰好使VO2+→VO2+,而Cr3+不变,此时MnO4→Mn2+,则原溶液中Cr的质量为( )
A.15.6mgB.23.4mgC.31.2mgD.46.8mg
【答案】D
【解析】
由信息滴入29.00mL0.1mol/L的FeSO4溶液,恰好使VO2+→VO2+,Cr2O72-→Cr3+,Fe元素的化合价升高,V、Cr元素的化合价降低;再滴入2.00mL,0.020mol/LKMnO4溶液,又恰好使VO2+→VO2+,而Cr3+不变,此时MnO4→Mn2+,Mn元素的化合价降低,V元素的化合价升高,则整个过程中Fe、Mn、Cr的化合价变化,设原溶液中Cr的质量为x,
由电子守恒可知,
29.00mL×10-3L×0.1mol/L×(3-2)=![]() ×(6-3)+2.00mL×10-3L×0.020mol/L×(7-2),解得x=46.8×10-3g=46.8mg,故D正确;
×(6-3)+2.00mL×10-3L×0.020mol/L×(7-2),解得x=46.8×10-3g=46.8mg,故D正确;
故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】将V1 mL1.00mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL,下列叙述正确的是( )
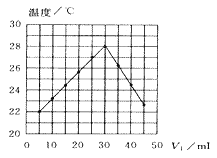
A.做该实验时环境温度为22℃
B.该实验表明化学能可能转化为热能
C.NaOH溶液的浓度约为1.00mol·L-1
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7
B.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能
C.高氯酸的酸性与氧化性均大于次氯酸的酸性与氧化性
D.邻羟基苯甲醛的熔点高于对羟基苯甲醛的熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呋喃酚是合成农药的重要中间体,其合成路线如下:
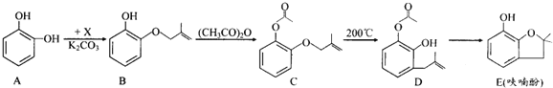
(1)A在空气中久置会由无色转变为棕褐色,其原因是____________,A在核磁共振氢谱中有___________组峰。
(2)B→C的反应类型是_____________________。
(3)已知X的分子式为C4H7Cl。写出A→B的化学方程式:___________________。
(4)要鉴别化合物C和D,适宜的试剂是__________________________。
(5)B的同分异构体很多,符合下列条件的有______种,写出其中能发生银镜反应的同分异构体的结构简式:__________(任写一种)。
①苯的衍生物 ②有两个互为对位的取代基 ③含有酯基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是NaCl、MgSO4的溶解度曲线。下列说法正确的是 ( )
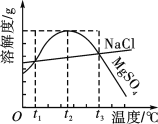
A. 只有在t1 ℃时,NaCl和MgSO4的溶解度才相等
B. t1~t2 ℃,MgSO4的溶解度随温度升高而减小
C. 在t2 ℃时,MgSO4饱和溶液的溶质质量分数最大
D. 把MgSO4饱和溶液的温度从t3 ℃降至t2 ℃时,有晶体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氧化性:BrO3->IO3->Br2>I2。向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加KBrO3的物质的量的关系如图所示。请回答下列问题:
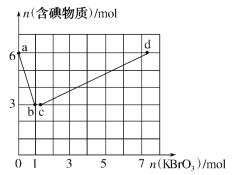
(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为__,还原产物是__。
(2)已知b→c过程中,仅有一种元素发生化合价变化,写出并配平该反应的离子方程式___。
(3)①已知反应:2BrO3-+I2→2IO3-+Br2;有同学由此得出氧化性:I2>Br2的结论,你认为是否正确___,并说明理由:___。
(4)计算c→d过程中消耗KBrO3的物质的量___。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp(CaSO4)=9×10-4,常温下CaSO4在水中的沉淀溶解平衡曲线如图所示。下列判断中正确的是( )
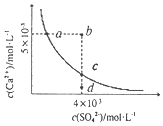
A.a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液
B.向d点溶液中加入适量CaCl2固体可以变到c点
C.a点对应的Ksp不等于c点对应的Ksp
D.b点将有沉淀生成,平衡后溶液中c(SO42-)=3×10-3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,用0.100 mol·L-1盐酸分别滴定20.00 mL 0.100 mol·L-1的NaHA和20.00 mL 0.100 mol·L-1 Na2A溶液,两溶液的pH与所加盐酸体积(V)的关系如图所示。下列说法正确的是( )
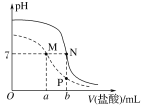
A.HA-的电离常数大于水解常数
B.b=2a
C.M、N点溶液均满足c(Na+)=2c(A2-)+c(HA-)
D.水的电离程度:M=N>P
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com