
常温下,在溶液中可发生以下反应:①2Fe2++Br2===2Fe3++2Br-,②2Br-+Cl2===Br2+2Cl-,③2Fe3++2I-===2Fe2++I2。由此判断下列说法错误的是
A.铁元素在反应①和③中均被氧化
B.反应②中当有1 mol Cl2被还原时,有2 mol Br-被氧化
C.氧化性强弱顺序:Cl2>Br2>Fe3+>I2
D.还原性强弱顺序:I->Fe2+>Br->Cl-
科目:高中化学 来源:2016届山东省高三上学期开学考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.用小苏打类药物治疗胃酸过多:HCO3-+H+==CO2↑+H2O
B.FeCl3溶液与Cu的反应:Cu+Fe3+==Cu2++Fe2+
C.向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:Ba2++OH-+H++SO42-==BaSO4↓+H2O
D.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+==Ca2++H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
下列应用及解释都正确的是
选项 | 应用 | 解释 |
A | 保存硫酸亚铁溶液需加入铁钉和少量稀盐酸 | 防止 Fe2+水解以及被 O2 氧化 |
B | 向滴有酚酞的 Na2CO3 溶液中加入 BaCl2溶液,溶液褪色 | BaCl2 有酸性 |
C | 在未知溶液中滴加 BaCl2 溶液出现白色沉淀,加稀硝酸,沉淀不溶解 | 该未知溶液中一定存在 SO42-或 SO32- |
D | 在相同条件下,向一支试管中加入 2 mL5%H2O2 和 1 mL H2O,向另一支试管中 加入 2mL 5% H2O2 和 1 mL FeCl3 溶液, 观察并比较实验现象 | 可以探究催化剂 FeCl3 对 H2O2 分解速 率的影响 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高一下学期期末考试化学试卷(解析版) 题型:选择题
空气是人类生存所必需的重要资源,为改善空气质量而启动的“蓝天工程”得到了全民支持.下列措施不利于“蓝天工程”建设的是
A.把燃煤的火力发电厂的烟囱造高,减少酸雨的污染
B.实施绿化工程,防治扬尘污染
C.为汽车安装尾气转化装置,消除机动车尾气污染
D.推广使用燃煤脱硫技术,防治SO2污染
查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上学期第一次月考化学试卷(解析版) 题型:填空题
【化学——选修2:化学与技术】(15分)丙酮和苯酚都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下:
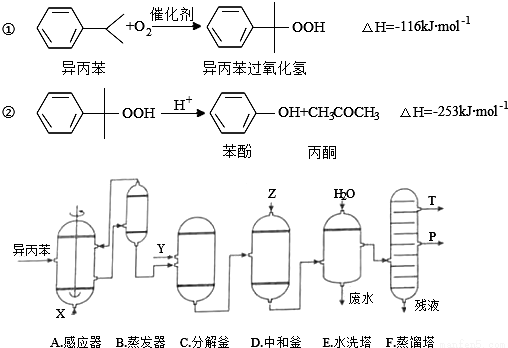
相关化合物的物理常数
物质 | 相对分子质量 | 密度(g/cm﹣3) | 沸点/℃ | ||
苯酚 | 94 | 1.0722 | 182 | ||
丙酮 | 58 | 0.7898 | 56.5 | ||
异丙苯 | 120 | 0.8640 | 153 | ||
回答下列问题:
(1)反应①和②分别在装置 和 中进行(填装置符号).
(2)反应②为 (填“放热”或“吸热”)反应.反应温度控制在50﹣60℃,温度过高的安全隐患是 .
(3)在反应器A中通入的X是 .
(4)在分解釜C中加入的Y为少量浓硫酸,其作用是 ,优点是用量少,缺点是 .
(5)中和釜D中加入的Z最适宜的是 (填编号.已知苯酚是一种弱酸)
a.NaOH b.CaCO3 c.NaHCO3 d.CaO
(6)蒸馏塔F中的馏出物T和P分别为 和 ,判断的依据是 .
(7)用该方法合成苯酚和丙酮的优点是 .
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三第一次月考化学试卷(解析版) 题型:选择题
有一澄清透明的溶液,只可能含有大量的Fe3+、Fe2+、H+、AlO2-、Al3+、CO32-、NO3-七种离子中的几种,向该溶液中逐滴加入一定量1 mol·L-1 NaOH溶液的过程中,开始没有沉淀,而后才有沉淀。则下列判断正确的是
A.溶液中可能含有AlO2- B.溶液中可能含有NO3-
C.溶液中一定不含Fe2+和Fe3+ D.溶液中可能含有Fe3+,但一定不含Fe2+
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三9月月考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是
A.向Fe2(SO4)3溶液中滴入KSCN溶液:Fe3++3SCN﹣ Fe(SCN)3↓
Fe(SCN)3↓
B.向NaHCO3溶液中滴加少量Ca(OH)2溶液:Ca2++OH﹣+HCO3﹣=CaCO3↓+H2O
C.向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42﹣+Ba2++2OH﹣=2H2O+BaSO4↓
D.用KIO3氧化酸性溶液中的KI:5I﹣+IO3﹣+3H2O=3I2+6OH﹣
查看答案和解析>>
科目:高中化学 来源:2016届河南省八市高三9月教学质量监测考试化学试卷(解析版) 题型:选择题
如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是
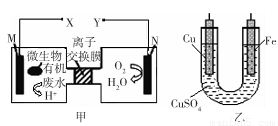
A.质子透过离子交换膜由右向左移动
B.铜电极应与X相连接
C.M电极反应式:

D.当N电极消耗0.25 mol气体时,则铁电极增重16 g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北正定中学高二上学期第一次联考化学试卷(解析版) 题型:选择题
部分弱电解质的电离平衡常数如下表,以下选项错误的是
化学式 | NH3·H2O | CH3COOH | HCN | H2CO3 |
Ki(25℃) | 1.8×l0—5 | 1.8×l0—5 | 4.9×l0—10 | Ki1= 4.3×l0—7 Ki2= 5.6×l0—11 |
A.等物质的量浓度的NaHCO3和NaCN溶液,前者溶液中水的电离程度大
B.0.1 mol/L CH3COONa 溶液显碱性,0.1 mol/L CH3COONH4 溶液显中性
C.CN-+H2O+CO2→HCN+ HCO3-
D.中和等体积、等pH的CH3COOH和HCN消耗NaOH的量前者小于后者
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com