
【题目】工业上联合生产碳酸氢钠和氯代烃的工艺流程如图所示,在生产NaHCO3的过程中完成乙烯氯化,下列叙述错误的是
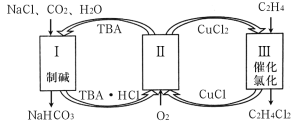
A.过程Ⅰ中的TBA替代了侯德榜制碱法中的氨气
B.在过程Ⅱ中实现了TBA、CuCl2的再生
C.理论上每生成1mol NaHCO3,可得到1mol C2H4Cl2
D.过程Ⅲ中的反应是C2H4+2CuCl2![]() C2H4Cl2+2CuCl
C2H4Cl2+2CuCl
【答案】C
【解析】
根据题意可知,制碱过程为NaCl+CO2+H2O+TBA=NaHCO3+TBAHCl,过程Ⅱ为TBA的再生过程为![]() O2+2CuCl+2TBAHCl=2CuCl2+2TBA+H2O,乙烯的氯化过程为C2H4+2CuCl2
O2+2CuCl+2TBAHCl=2CuCl2+2TBA+H2O,乙烯的氯化过程为C2H4+2CuCl2![]() C2H4Cl2+2CuCl,由此分析。
C2H4Cl2+2CuCl,由此分析。
A.侯德榜制碱法是先把氨气通入食盐水,然后向氨盐水中通二氧化碳,生产溶解度较小的碳酸氢钠,再将碳酸氢钠过滤出来,经焙烧得到纯净洁白的碳酸钠,由图可知,过程I中的TBA替代了侯德榜制碱法中的氨气,故A正确;
B.程Ⅱ为TBA的再生过程为![]() O2+2CuCl+2TBAHCl=2CuCl2+2TBA+H2O,实现了TBA、CuCl2的再生,故B正确;
O2+2CuCl+2TBAHCl=2CuCl2+2TBA+H2O,实现了TBA、CuCl2的再生,故B正确;
C.制碱过程为NaCl+CO2+H2O+TBA=NaHCO3+TBAHCl,理论上每生成1mol NaHCO3需要1mol TBA,根据过程Ⅱ为TBA的再生过程为![]() O2+2CuCl+2TBAHCl=2CuCl2+2TBA+H2O,乙烯的氯化过程为C2H4+2CuCl2
O2+2CuCl+2TBAHCl=2CuCl2+2TBA+H2O,乙烯的氯化过程为C2H4+2CuCl2![]() C2H4Cl2+2CuCl,则关系式TBACuCl
C2H4Cl2+2CuCl,则关系式TBACuCl![]() C2H4Cl2,则理论上每生成1mol NaHCO3,可得到0.5mol C2H4Cl2,故C错误;
C2H4Cl2,则理论上每生成1mol NaHCO3,可得到0.5mol C2H4Cl2,故C错误;
D.根据分析,过程Ⅲ是乙烯的氯化过程,化学方程式为C2H4+2CuCl2![]() C2H4Cl2+2CuCl,故D正确;
C2H4Cl2+2CuCl,故D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】化合物Z是合成某种抗结核候选药物的重要中间体,可由下列反应制得。
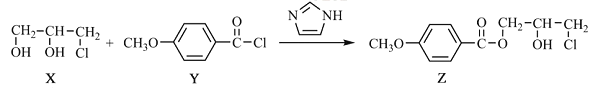
下列有关化合物X、Y和Z的说法正确的是
A.X分子中不含手性碳原子
B.Y分子中的碳原子一定处于同一平面
C.Z在浓硫酸催化下加热可发生消去反应
D.X、Z分别在过量NaOH溶液中加热,均能生成丙三醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 碳酸钡与盐酸反应2H++BaCO3===Ba2++H2O+CO2↑
B. 氢氧化钡溶液与稀硫酸混合Ba2++![]() +H++OH-===BaSO4↓+H2O
+H++OH-===BaSO4↓+H2O
C. 金属钠与水的反应 Na+H2O===Na++OH-+H2↑
D. 铜片插入硝酸银溶液中:Cu + Ag+ = Cu2+ + Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中:
a. 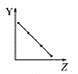 b.
b. 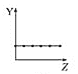 c.
c. 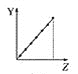 d.
d. 
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为___________(名称),Y为____________(元素符号),Z原子结构示意图为________________。
②N的最高价氧化物的水化物的化学式为________________。
③M的最高价氧化物的化学式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)是制造LED的重要材料,被誉为“第三代半导体材料”。镓(31Ga)的氧化物和氢氧化物均为两性化合物,工业制备氮化镓的工艺流程如图所示。下列判断正确的是
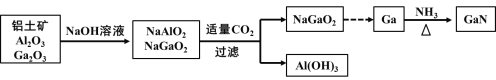
A.Ga位于第五周期第IIIA族B.酸性:Al(OH)3>Ga(OH)3
C.Ga(OH)3可与NaOH反应生成NaGaO2D.Ga与NH3反应的另一种生成物可用作航天燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝和氢氧化钠都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是___________________________________________。
(2)可用阳离子交换膜法电解饱和食盐水制NaOH,其工作原理如左下图所示。
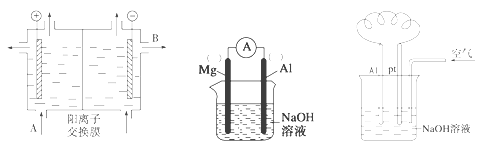
①请写出A、B两处物质的名称或化学式:A___________________、B____________________
②请写出电解食盐水的离子方程式__________________________________________
(3)以镁条、铝片为电极,以NaOH溶液为电解质溶液设计的原电池如上中图。
①负极材料为________(填Mg或Al)。
②该原电池的总反应式为____________________________________________
(4)铝—空气燃料电池可用于电动汽车,通常以NaOH溶液为电解液,铝合金为负极,通入空气的极为正极(如右上图),则
负极的电极反应式为__________________________________;
正极的电极反应式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告提出要对环境问题进行全面、系统的可持续治理。绿色能源是实施可持续发展的重要途径,利用生物乙醇来制取绿色能源氢气的部分反应过程如下图所示:

(1)已知:CO(g) +H2O(g)CO2(g)+H2(g) H1=-41 kJ·mol-1
CH3CH2OH(g)+3H2O(g)2CO2(g)+6H2(g) H2 =+174.1 kJ·mol-1
反应I的热化学方程式为______。
(2)反应II在进气比[n(CO) : n(H2O)]不同时,测得相应的 CO 平衡转化率见下图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。

①图中A、E和 G三点对应的反应温度TA、TE、TG的关系是_____,其原因是 ______。该温度下,要提高CO平衡转化率,除了改变进气比之外,还可采取的措施是______。
②由图中可知CO的平衡转化率与进气比、反应温度之间的关系是____。
③A、B 两点对应的反应速率大小:vA_____vB(填“<” “=”或“>”)。已知反应速率 v=v正v逆= k正x(CO)x(H2O) k逆x(CO2) x(H2) ,k为反应速率常数,x为物质的量分数,在达到平衡状态为D点的反应过程中,当CO的转化率刚好达到20%时,![]() =_____。
=_____。
(3)反应III在饱和KHCO3电解液中,电解活化的CO2来制备乙醇,其原理如图所示,则阴极的电极反应式为___________。
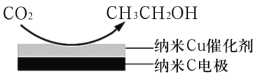
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0。某温度下,将2molSO2和1molO2置于10L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g) ΔH<0。某温度下,将2molSO2和1molO2置于10L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

A.由图甲知,A点SO2的平衡浓度为0.08mol·L-1
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2
C.达到平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示
D.压强为0.50MPa时不同温度下SO2的转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Pd/A12O3是常见的汽车尾气催化剂。一种从废Pd/A12O3纳米催化剂(主要成分及含量:Pd0.3%,γ-A12O392.8%,其他杂质6.0%)中回收金属Pd的工艺:

已知:γ-Al2O3能与酸反应,α-A12O3不与酸反应。
回答下列问题:
(1)“预处理”时,γ-A12O3经焙烧转化为α-A12O3,该操作的主要目的是_________。
(2)“酸浸”时,Pd转化为PdCl42-,其离子方程式为_________。
(3)“滤液①”和“滤液②”中都含有的主要溶质有_________(填化学式)。
(4)“粗Pd”溶解时,可用稀HNO3替代NaClO3,但缺点是_________。两者相比,_________(填化学式)的氧化效率更高(氧化效率以单位质量得到的电子数表示)。
(5)“沉淀”时,[Pd(NH3)4]2+转化为[Pd(NH3)2]Cl2沉淀,其化学方程式为_________。
(6)酸性条件下,BrO3-能在负载Pd/A12O3纳米催化剂的电极表面快速转化为Br-。
①发生上述转化反应的电极应接电源的_________极(填“正”或“负”);
②研究表明,电流密度越大,电催化效率越高;但当电流密度过大时,该电极会发生副反应生成_________填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com