
| A. | 镁离子的电子式Mg2+ | B. | Cl的结构示意图 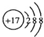 | ||
| C. | 氯离子的电子式Cl- | D. | 质量数为37的氯原子${\;}_{37}^{17}$Cl |
分析 A.镁离子为简单阳离子,其电子式直接用离子符号表示;
B.氯原子的核电荷数=核外电子总数=17,最外层含有7个电子;
C.氯离子为阴离子,电子式中需要标出最外层电子;
D.元素符号的最简式为质量数、左下角为质子数.
解答 解:A.镁离子为简单阳离子,其电子式为Mg2+,故A正确;
B.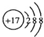 为氯离子结构示意图,氯原子的最外层电子数为7,正确的原子结构示意图为:
为氯离子结构示意图,氯原子的最外层电子数为7,正确的原子结构示意图为: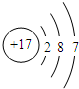 ,故B错误;
,故B错误;
C.氯离子为阴离子,电子式中需要标出其最外层电子,氯离子正确的电子式为: ,故C错误;
,故C错误;
D.氯原子的质子数为17,质量数为37的氯原子的正确表示方法为:1737Cl,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、原子结构示意图与离子结构示意图、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题侧重考查学生的规范答题能力.


科目:高中化学 来源: 题型:多选题
| A. | 由反应:2Fe2++Cl2→2Fe3++2Cl-,可以得出还原性Cl2<Fe3+ | |
| B. | 由于钢铁表面水膜里溶有氧气和二氧化碳,所以日常的金属腐蚀以析氢腐蚀为主 | |
| C. | 将钢铁接在外电源的负极上,另一金属(不是惰性金属)接在外电源的正极上组成电解池,可以防钢铁腐蚀 | |
| D. | 纯锌与稀硫酸反应比不纯的锌(一般含铁、铜等杂质)与相同的稀硫酸反应慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ( D)=0.4 mol/(L•s) | B. | v( C)=0.8mol/(L•s) | C. | υ( B)=0.6 mol/(L•s) | D. | υ( A)=0.5 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+HCl $→_{△}^{催化剂}$ CH3CH2Cl | |
| B. | CH4+Cl2 $\stackrel{光}{→}$CH3Cl+HCl | |
| C. | nCH2=CH2$→_{加热、加压}^{催化剂}$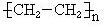 | |
| D. | CH3CH2Br+NaOH$→_{△}^{乙醇}$CH2=CH2↑+NaBr+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaO | B. | CO | C. | SiO2 | D. | H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com