
平衡密闭容器中,加入一定量的X和Y,发生如下反应:2X(?)+Y(?)![]() 2Z(?),不同温度时产物Z的生成情况如右图所示:a为T1℃时的情况,b为T2℃时的情况,c为T2℃时从时间t3开始向容器中加压的情况。下列叙述正确的是( )
2Z(?),不同温度时产物Z的生成情况如右图所示:a为T1℃时的情况,b为T2℃时的情况,c为T2℃时从时间t3开始向容器中加压的情况。下列叙述正确的是( )

A.X、Y、Z均为气体,正反应放热
B.Y、Z为气体,X为非气体,正反应放热
C.Z为气体,X、Y中至少有一种为非气体,正反应放热
D.t4时刻气体的平均相对分子质量可能小于t3时刻气体的平均相对分子质量
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
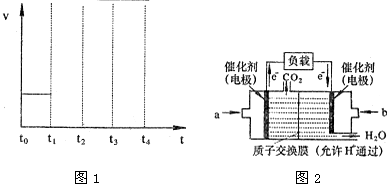
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(X)/mol?L-1 容器体积/L 温度/℃ |
1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
| A、m>n |
| B、温度不变,增大体积,X的转化率增大 |
| C、Q<0 |
| D、体积不变,温度升高,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源:2010—2011学年浙江省金华十校高二下学期期中考试化学试卷 题型:单选题
平衡密闭容器中,加入一定量的X和Y,发生如下反应:2X(g)+Y(g)=2Z(g),不同温度时产物Z的生成情况如右图所示:a为T1℃时的情况,b为T2℃时的情况,c为T2℃时从时间t3开始向容器中加压的情况。下列叙述正确的是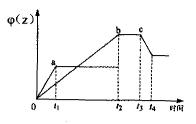
| A.X、Y、Z均为气体,正反应放热 |
| B.Y、Z为气体,X为非气体,正反应放热 |
| C.Z为气体,X、Y中至少有一种为非气体,正反应放热 |
| D.t4时刻气体的平均相对分子质量可能小于t3时刻气体的平均相对分子质量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com