
”¾ĢāÄæ”æ£Ø1£©ŅŃÖŖijĘųĢ¬Ģžŗ¬Ģ¼85.7%£¬ŌŚ±ź×¼×“æöĻĀ£¬øĆĘųĢ¬ĢžµÄĆܶČĪŖ1.875g/L”£øĆĘųĢå·Ö×ÓæÉÄܵĽį¹¹¼ņŹ½ĪŖ
£Ø2£©ĒėøųĻĀĆęµÄÓŠ»śĪļĆüĆū ”£CH3CH2C(CH3£©2C(CH2CH3£©2CH3
£Ø3£©µ±0.2molĢžAŌŚ×ćĮæŃõĘųÖŠĶźČ«Č¼ÉÕŹ±Éś³ÉCO2ŗĶH2Oø÷1.2mol£¬“߻ƼÓĒāŗóÉś³É2£¬2£¶ž¼×»ł¶”Ķ飬ŌņAµÄ½į¹¹¼ņŹ½ĪŖ ”£
£Ø4£©Ä³ĶéĢžµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ72£¬Čō“ĖÓŠ»śĪļµÄŅ»ĀČ“śĪļ·Ö×ÓÖŠŗ¬ÓŠĮ½øö£CH3£¬Į½øö£CH2££¬Ņ»øö ![]() ŗĶŅ»øö£Cl£¬ĖüµÄæÉÄܽį¹¹ÓŠĖÄÖÖ£¬ĒėŠ“³öĖüĆĒµÄ½į¹¹¼ņŹ½£ŗ ”£
ŗĶŅ»øö£Cl£¬ĖüµÄæÉÄܽį¹¹ÓŠĖÄÖÖ£¬ĒėŠ“³öĖüĆĒµÄ½į¹¹¼ņŹ½£ŗ ”£
”¾“š°ø”æ£Ø1£©CH2=CH-CH3£¬![]()
£Ø2£©3,3,4-Čż¼×»ł-3-ŅŅ»ł¼ŗĶé £Ø3£©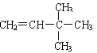
£Ø4£©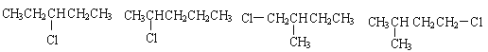
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©ŌŚ±ź×¼×“æöĻĀ£¬ĘųĢ¬ĢžµÄĆܶČĪŖ1.875g/L£¬ŌņøĆĢžµÄĦ¶ūÖŹĮæĪŖ22.4L/mol”Į1.875g/L=42g/mol£¬øł¾ŻøĆĢžŗ¬Ģ¼85.7%æɵĆCŌ×ÓøöŹżĪŖ£ŗ![]() =3£¬ĖłŅŌHŌ×ÓøöŹżĪŖ£ŗ
=3£¬ĖłŅŌHŌ×ÓøöŹżĪŖ£ŗ![]() =6£¬Ņņ“Ė·Ö×ÓŹ½ĪŖC3H6£¬æÉÄÜĪŖĻ©Ģž»ņ»·ĶéĢž£¬æÉÄܵĽį¹¹¼ņŹ½ĪŖCH2=CH-CH3»ņ
=6£¬Ņņ“Ė·Ö×ÓŹ½ĪŖC3H6£¬æÉÄÜĪŖĻ©Ģž»ņ»·ĶéĢž£¬æÉÄܵĽį¹¹¼ņŹ½ĪŖCH2=CH-CH3»ņ![]() ”£
ӣ
£Ø2£©øł¾ŻĶéĢžµÄĻµĶ³ĆüĆū·ØĆüĆū”£CH3CH2C(CH3£©2C(CH2CH3£©2CH3µÄĆū³ĘĪŖ3,3,4-Čż¼×»ł-3-ŅŅ»ł¼ŗĶ锣
£Ø3£©µ±0.2molĢžAŌŚ×ćĮæŃõĘųÖŠĶźČ«Č¼ÉÕŹ±Éś³ÉCO2ŗĶH2Oø÷1.2mol£¬ÕāæÉŅŌČ·¶ØAÖŠ6øöCŗĶ12øöH£¬·Ö×ÓŹ½ĪŖC6H12£¬²»±„ŗĶ¶ČĪŖ1£¬ÓŠŅ»øöĢ¼Ģ¼Ė«¼ü”£ÓÖŅņĪŖ¼Ó³É²śĪļĪŖ2£¬2£¶ž¼×»ł¶”Ķ飬¹ŹAĪŖ3£¬3£¶ž¼×»ł-1-¶”Ļ©£¬½į¹¹¼ņŹ½ĪŖ ”£
ӣ
£Ø4£©Ä³ĶéĢžµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ72£¬ŌņøĆĶéĢžµÄ·Ö×ÓŹ½ĪŖC5H12£¬Čō“ĖÓŠ»śĪļµÄŅ»ĀČ“śĪļ·Ö×ÓÖŠŗ¬ÓŠĮ½øö£CH3£¬Į½øö£CH2££¬Ņ»øö ![]() ŗĶŅ»øö£Cl£¬æÉÄܽį¹¹¼ņŹ½ĪŖ
ŗĶŅ»øö£Cl£¬æÉÄܽį¹¹¼ņŹ½ĪŖ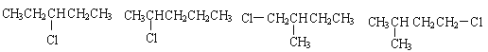 ”£
ӣ


 °ŁÄźŃ§µäæĪŹ±Ń§Į·²āĻµĮŠ“š°ø
°ŁÄźŃ§µäæĪŹ±Ń§Į·²āĻµĮŠ“š°ø ČŹ°®Ó¢ÓļĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø
ČŹ°®Ó¢ÓļĶ¬²½Į·Ļ°²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ0.1 mol”¤L-1 NH3”¤H2OČÜŅŗÖŠ“ęŌŚČēĻĀµēĄėĘ½ŗā£ŗNH3”¤H2O![]() NH4+ + OH- ”£¶ŌÓŚøĆĘ½ŗā£¬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
NH4+ + OH- ”£¶ŌÓŚøĆĘ½ŗā£¬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A. ¼ÓČėĖ®Ź±£¬ČÜŅŗÖŠc(OH-) / c(NH3”¤H2O) Ōö“ó
B. ¼ÓČėÉŁĮæNaOH¹ĢĢå£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬µēĄėĘ½ŗā³£Źż¼õŠ”
C. ¼ÓČėÉŁĮæ0.1 mol”¤L-1 HClČÜŅŗ£¬ČÜŅŗÖŠc(OH-)Ōö“ó
D. ½µµĶĪĀ¶Č£¬ČÜŅŗÖŠc(NH4+)Ōö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬²»ŹōÓŚ“¼ĄąµÄŹĒ£Ø £©
A. C4H9OH B. C6H5CH2OH C. C6H5OH D. øŹÓĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬ĻĀĮŠø÷×éĪļÖŹÖŠ£¬Y¼ČÄÜÓėX·“Ó¦ÓÖÄÜÓėZ·“Ó¦µÄŹĒ
X | Y | Z | |
¢Ł | NaOHČÜŅŗ | Al(OH)3 | Ļ”ĮņĖį |
¢Ś | KOHČÜŅŗŅŗ | Na2CO3 | Ļ”ŃĪĖį |
¢Ū | CO2 | Na2O2 | H2O |
¢Ü | FeCl3ČÜŅŗ | Cu | Ļ”ĮņĖį |
A. ¢Ł¢Ū B. ¢Ł¢Ü C. ¢Ś¢Ü D. ¢Ś¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij³§·ĻĖ®ÖŠŗ¬5.00”Į10-3mol”¤L-1µÄCr2O72-£¬Ę䶾ŠŌ½Ļ“ó”£Ä³ŃŠ¾æŠŌѧĻ°Š”×éĪŖĮĖ±ä·ĻĪŖ±¦£¬½«·ĻĖ®“¦ĄķµĆµ½“ÅŠŌ²ÄĮĻCr0.5Fe1.5FeO4£ØFeµÄ»ÆŗĻ¼ŪŅĄ“ĪĪŖ+3”¢+2£©£¬Éč¼ĘĮĖČēĻĀŹµŃéĮ÷³Ģ£ŗ
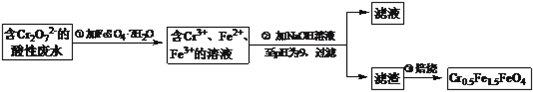
£Ø1£©µŚ¢Ł²½·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ____________________£»
£Ø2£©µŚ¢Ś²½ÖŠÓĆpHŹŌÖ½²ā¶ØČÜŅŗpHµÄ²Ł×÷ŹĒ£ŗ________________£»
£Ø3£©µŚ¢Ś²½¹żĀĖµĆµ½µÄĀĖŌüÖŠÖ÷ŅŖ³É·Ö³żCr(OH)3Ķā£¬»¹ÓŠ____________£»
£Ø4£©ÓūŹ¹1LøĆ·ĻĖ®ÖŠCr2O72-µÄĶźČ«×Ŗ»ÆĪŖCr0.5Fe1.5FeO4”£ĄķĀŪÉĻŠčŅŖ¼ÓČė____FeSO4”¤7H2O”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æėĀ(N2H4)Ķس£ÓĆ×÷»š¼żµÄøßÄÜČ¼ĮĻ£¬N2O4 ×÷Ńõ»Æ¼Į”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ÅŅŃÖŖ£ŗN2(g)+2O2(g)=2NO2(g) ”÷H=+a kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) ”÷H=-b kJ/mol
2NO2(g)![]() N2O4(g) ”÷H=-c kJ/mol
N2O4(g) ”÷H=-c kJ/mol
Š“³öĘųĢ¬ėĀŌŚĘųĢ¬ N2O4 ÖŠČ¼ÉÕÉś³ÉµŖĘųŗĶĘųĢ¬Ė®µÄČČ»Æѧ·½³ĢŹ½ ”£
¢Ę¹¤ŅµÉĻ³£ÓĆ“ĪĀČĖįÄĘÓė¹żĮæµÄ°±Ęų·“Ó¦ÖʱøėĀ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
¢ĒN2”¢H2 ŗĻ³É°±ĘųĪŖ·ÅČČ·“Ó¦”£800K Ź±ĻņĻĀĮŠĘšŹ¼Ģå»żĻąĶ¬µÄĆܱÕČŻĘ÷ÖŠ³äČė 2mol N2”¢3mol H2£¬ ¼×ČŻĘ÷ŌŚ·“Ó¦¹ż³ĢÖŠ±£³ÖŃ¹Ēæ²»±ä£¬ŅŅČŻĘ÷±£³ÖĢå»ż²»±ä£¬±ūŹĒ¾ųČČČŻĘ÷£¬ČżČŻĘ÷ø÷×Ō½ØĮ¢»ÆŃ§Ę½ŗā”£

“ļµ½Ę½ŗāŹ±£¬Ę½ŗā³£Źż K ¼× K ŅŅ(Ģī”°©”±”°©”±»ņ”°=”±)”£
¢Ś “ļµ½Ę½ŗāŹ± N2 µÄÅØ¶Č c(N2)ŅŅ c(N2)±ū(Ģī”°©”±”°©”±»ņ”°=”±)”£
¢Ū ¶Ō¼×”¢ŅŅ”¢±ūȿȯĘ÷µÄĆčŹö£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ŅŅČŻĘ÷ĘųĢåĆÜ¶Č²»ŌŁ±ä»ÆŹ±£¬ĖµĆ÷“Ė·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬
B. ŌŚ¼×ÖŠ³äČėĻ”ÓŠĘųĢå He£¬»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ
C. ½«¼×ÖŠµÄ»īČūĶłĻĀŃ¹ÖĮŌĢå»żµÄŅ»°ė£¬Ę½ŗāĻņÓŅŅʶÆ
D.±ūČŻĘ÷ĪĀ¶Č²»ŌŁ±ä»ÆŹ±ĖµĆ÷ŅŃ“ļĘ½ŗāדĢ¬
¢Č °±ĘųĶØČėČēĶ¼µē½ā×°ÖĆæÉŅŌøØ֜ɜ²ś NH4NO3£¬øƵē½ā³ŲŅõ¼«·“Ó¦Ź½ĪŖ ”£

¢É ŌŚ 20mL 0.2mol/L µÄ NH4NO3 ČÜŅŗÖŠ¼ÓČė 10mL 0.2mol/L NaOH ČÜŅŗŗóĻŌ¼īŠŌ£¬ČÜŅŗÖŠĖłÓŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ[ĪļÖŹ½į¹¹ÓėŠŌÖŹ]ŃõŌŖĖŲŗĶĀ±×åŌŖĖŲ¶¼ÄÜŠĪ³É¶ąÖÖĪļÖŹ£¬ĪŅĆĒæÉŅŌĄūÓĆĖłŃ§ĪļÖŹ½į¹¹ÓėŠŌÖŹµÄĻą¹ŲÖŖŹ¶Č„ČĻŹ¶ŗĶĄķ½ā”£
£Ø1£©äåµÄ¼Ūµē×ÓÅŲ¼Ź½ĪŖ £»PCl3µÄæռ乹ŠĶĪŖ ”£
£Ø2£©ŅŃÖŖCsICl2²»ĪČ¶Ø£¬ŹÜČČŅ×·Ö½ā£¬ĒćĻņÓŚÉś³É¾§øńÄÜøü“óµÄĪļÖŹ£¬ŌņĖü°“ĻĀĮŠ Ź½·¢Éś:
A£®CsICl2=CsCl+ICl B£®CsICl2=CsI+Cl2
£Ø3£©øł¾ŻĻĀ±ķµŚŅ»µēĄėÄÜŹż¾ŻÅŠ¶Ļ£ŗ×īÓŠæÉÄÜÉś³É½ĻĪČ¶ØµÄµ„ŗĖŃōĄė×ÓµÄĀ±ĖŲŌ×ÓŹĒ__________
·ś | ĀČ | äå | µā | |
µŚŅ»µēĄėÄÜ£ØkJmol©1£© | 1681 | 1251 | 1140 | 1008 |
£Ø4£©ĻĀĮŠ·Ö×Ó¼Č²»“ęŌŚs©p¦Ņ¼ü£¬Ņ²²»“ęŌŚp©p¦Š¼üµÄŹĒ
A£® HCl B£®HF C£® SO2 D£® SCl2
£Ø5£©ŅŃÖŖCOCl2ĪŖĘ½ĆęŠĪ£¬ŌņCOCl2ÖŠŠÄĢ¼Ō×ÓµÄŌӻƹģµĄĄąŠĶĪŖ £¬Š“³öCOµÄµČµē×ÓĢåµÄĪ¢Į£ £ØŠ“³ö1øö£©”£
£Ø6£©øĘŌŚŃõĘųÖŠČ¼ÉÕŹ±µĆµ½Ņ»ÖÖøʵÄŃõ»ÆĪļ¾§Ģ壬Ęä½į¹¹ČēĶ¼ĖłŹ¾£ŗÓÉ“ĖæÉÅŠ¶ĻøĆøʵÄŃõ»ÆĪļµÄ»Æѧ Ź½ĪŖ ”£ŅŃÖŖøĆŃõ»ÆĪļµÄĆܶȏĒ¦Ńgcm©3£¬Ōņ¾§°ūĄėµĆ×ī½üµÄĮ½øöøĘĄė×Ó¼äµÄ¾ąĄėĪŖ cm£ØÖ»ŅŖĒóĮŠĖćŹ½£¬²»±Ų¼ĘĖć³öŹżÖµ£¬°¢·ü¼ÓµĀĀŽ³£ŹżĪŖNA£©”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒŌŖĖŲÖÜĘŚ±ķÖŠ½ŲČ”µÄŅ»øöʬ¶Ī,ĘäÖŠX”¢Y”¢Z”¢W¾łŹōÓŚ¶ĢÖÜĘŚŌŖĖŲ”£Ēė»Ų“šĻĀĮŠĪŹĢā:
![]()
(1)ČōXµ„ÖŹĪŖæÕĘųµÄÖ÷ŅŖ³É·ÖÖ®Ņ»,ŌņWŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ”””””””””£
(2)ČōY”¢W”¢ZµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļŅĄ“ĪĪŖŅ»ŌŖĖį”¢¶žŌŖĖį”¢ČżŌŖĖį,ÕāČżÖÖĖįµÄÕżŃĪµÄŗ¬ŃõĖįøłĄė×ÓÖŠ,ÓŠĮ½Öֵĵē×ÓŹżĻąµČ,ŌņÕāĮ½ÖÖĄė×ӵķūŗÅŹĒ”””””””””¢”””””””””£
(3)ČōNaÓėYŗĶZµÄµ„ÖŹ·Ö±š·“Ó¦æÉŅŌÉś²śÄ¦¶ūÖŹĮæĻąĶ¬µÄĮ½ÖÖ»ÆŗĻĪļ,ĘäÖŠNaÓėYŠĪ³ÉµÄ»ÆŗĻĪļµÄµē×ÓŹ½ĪŖ””””””””””””””,Ėłŗ¬»Æѧ¼üµÄĄąŠĶĪŖ””
(4)YŌŖĖŲŌŚÖÜĘŚ±ķÖŠæÉÄÜ“¦ÓŚµŚ””””””””””””””””ׯŠŠ(Š“³öĖłÓŠæÉÄÜׯŠŠŹż)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĄė×ÓŌŚĪŽÉ«ČÜŅŗÖŠÄÜ“óĮæ¹²“ęµÄŹĒ
A. K+ӢFe3+ӢCl- B. K+ӢAlO2-ӢOH-
C. Na+ӢHCO3-ӢOH- D. Na+ӢCO32-ӢH+
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com