
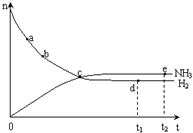
 �ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����壮 �ϳ����з�����ӦΪ��N2��g��+3H2��g��?2NH3��g����H��0
�ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ�����壮 �ϳ����з�����ӦΪ��N2��g��+3H2��g��?2NH3��g����H��0| T/K | T1 | 573 | T2 |
| K | 1.00��107 | 2.45��105 | 1.88��103 |
| c(H2)?c(CO2) |
| c(CO)?c(H2O) |
| 0.12��0.12 |
| 0.08��0.08 |
| x2 |
| (0.3-x)2 |
| 0.15 |
| 0.3 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� | �����Ϣ |
| X | ��̬ԭ�����������Ų�Ϊnsnnpn+1 |
| Y | ��ԭ��L���������K���3�� |
| Z | �䵥��������ˮ���ҷ�Ӧ�����ɵ��������ӵ�������ͬ |
| W | �䵥����Y2��ȼ�գ���������������ɫ���� |
| T | ���������������۵Ĵ�����Ϊ6 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢� | B���ڢ� | C���٢� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪CO2����������ɫȼ�ϼ״���CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-187.4kJ/mol��3000Cʱ�ĺ����ܱ������У���C��CO2��=1.00mol��L-1C��H2��=1.60mol��L-1��ʼ��Ӧ�������ͼ��ʾ���ش��������⣺
��֪CO2����������ɫȼ�ϼ״���CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-187.4kJ/mol��3000Cʱ�ĺ����ܱ������У���C��CO2��=1.00mol��L-1C��H2��=1.60mol��L-1��ʼ��Ӧ�������ͼ��ʾ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ij����Һ����AgNO3��Һ�����ɰ�ɫ������˵��ԭ��Һ����Cl- |
| B��ij����Һ����BaCl2��Һ�����ɰ�ɫ������˵��ԭ��Һ����SO42- |
| C��ij����Һ����CaCl2��Һ�����ɰ�ɫ������˵��ԭ��Һ����CO32- |
| D��ij����Һ����NaOH��Һ��������ɫ������˵��ԭ��Һ����Cu2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B��Ư�� |
| C������ | D���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ��1mol NO2��g����1mol CO��g����Ӧ����CO2��NO�����е������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��
��ͼ��1mol NO2��g����1mol CO��g����Ӧ����CO2��NO�����е������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com