

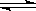 HA + OH-(2分) > (1分)
HA + OH-(2分) > (1分) 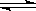 HA + OH-。HA是弱酸,抑制水的电离,而水解促进水的电离,所以混合溶液中由水电离出的c(H+)>0.2 mol/L HA溶液中由水电离出的c(H+)。
HA + OH-。HA是弱酸,抑制水的电离,而水解促进水的电离,所以混合溶液中由水电离出的c(H+)>0.2 mol/L HA溶液中由水电离出的c(H+)。

科目:高中化学 来源:不详 题型:单选题
| A.0.1 mol·L-1的盐酸和pH=13的氢氧化钡溶液等体积混合 |
| B.0.1 mol·L-1的NaHCO3溶液和pH=1的盐酸等体积混合 |
| C.pH=3的硫酸和pH=11的氨水等体积混合 |
| D.pH=1的醋酸和0.1mol/L的氢氧化钠溶液等体积混合 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③④⑥ | B.④⑤⑥ | C.①②④⑥ | D.②③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.原来盐酸的物质的量浓度为1mol·L-1 |
| B.X为0.1mol·L-1的NaOH溶液 |
| C.原来盐酸的物质的量浓度为0.1mol·L-1 |
| D.X为0.01mol·L-1的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通过沉淀反应,可以使溶液中某种离子的浓度变为0 |
| B.反应NH3+H3O+ |
| C.若测得雨水的pH小于7,则下的是酸雨 |
| D.先将pH试纸用蒸馏水润湿后,再测定溶液的pH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.PH=3的盐酸和PH=11的氨水等体积混合 |
| B.PH=3的盐酸和PH=11的氢氧化钡等体积混合 |
| C.PH=3的醋酸和PH=11的氢氧化钡等体积混合 |
| D.PH=3的硫酸和PH=11的氨水等体积混合 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.固体CH3COOK | B.固体CH3COONH4 | C.气体NH3 | D.固体NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com