
【题目】FeCO3与砂糖混用可作补血剂。以黄铁矿烧渣(含CuO、Fe2O3、FeO、SiO2、Al2O3等)为主要原料制备FeCO3的流程如下:
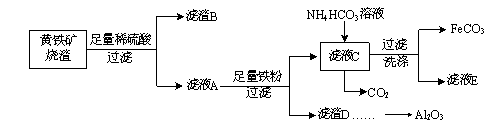
(1)质量分数为30%(密度是1.176 g·cm-3)的稀硫酸的物质的量浓度为 。
(2)检验滤液A中存在Fe2+的试剂是 。
(3)加入足量铁粉的作用除调节pH使Al3+转化为Al(OH)3沉淀外,还有两个作用,写出其中一个反应的离子方程式: 。
(4)写出滤液C与NH4HCO3溶液反应的离子方程式: 。
(5)FeCO3在空气中灼烧可制得铁系氧化物材料。已知25℃,101 kPa时:
4Fe(s)+3O2(g)![]() 2Fe2O3 ΔH=﹣1648 kJ·mol-1
2Fe2O3 ΔH=﹣1648 kJ·mol-1
C(s)+O2(g)![]() CO2(g) ΔH=﹣393 kJ·mol-1
CO2(g) ΔH=﹣393 kJ·mol-1
2Fe(s)+2C(s)+3O2(g)![]() 2FeCO3(s) ΔH=﹣1480 kJ·mol-1
2FeCO3(s) ΔH=﹣1480 kJ·mol-1
写出FeCO3在空气中灼烧生成Fe2O3的热化学方程式: 。
(6)某兴趣小组为充分利用副产品,欲利用滤渣D为原料制取Al2O3,请补充完成实验步骤:向滤渣D中加入适量NaOH溶液, 。
【答案】(1)3.6mol·L-1(2)酸性KMnO4溶液
(3)Fe+2Fe3+=3Fe2+(或Fe+Cu2+=Fe2++Cu)
(4)Fe2++2HCO![]() =FeCO3↓+CO2↑+H2O
=FeCO3↓+CO2↑+H2O
(5)4FeCO3(s)+O2(g)![]() 2Fe2O3(s)+4CO2(g)ΔH=﹣260kJ·mol-1
2Fe2O3(s)+4CO2(g)ΔH=﹣260kJ·mol-1
(6)过滤,向滤液中通入足量CO2,过滤并洗涤沉淀,加热所得沉淀至恒重
【解析】
试题分析:(1)根据![]() ,质量分数为30%(密度是1.176 g·cm-3)的稀硫酸的物质的量浓度为
,质量分数为30%(密度是1.176 g·cm-3)的稀硫酸的物质的量浓度为![]() 3.6 mol·L-1;(2)Fe3+没有还原性,Fe2+具有还原性,检验滤液A中存在Fe2+的试剂是酸性KMnO4溶液;(3)加入足量铁粉的作用除调节pH使Al3+转化为Al(OH)3沉淀,同时防止Fe2+被氧化,除去杂质铜离子,反应的离子方程式:Fe+2Fe3+=3Fe2+、Fe+Cu2+=Fe2++Cu;(4)根据图示,滤液C与NH4HCO3溶液反应生成碳酸亚铁和二氧化碳,离子方程式为Fe2++2HCO
3.6 mol·L-1;(2)Fe3+没有还原性,Fe2+具有还原性,检验滤液A中存在Fe2+的试剂是酸性KMnO4溶液;(3)加入足量铁粉的作用除调节pH使Al3+转化为Al(OH)3沉淀,同时防止Fe2+被氧化,除去杂质铜离子,反应的离子方程式:Fe+2Fe3+=3Fe2+、Fe+Cu2+=Fe2++Cu;(4)根据图示,滤液C与NH4HCO3溶液反应生成碳酸亚铁和二氧化碳,离子方程式为Fe2++2HCO![]() =FeCO3↓+CO2↑+H2O;(5)FeCO3在空气中灼烧可制得铁系氧化物材料。
=FeCO3↓+CO2↑+H2O;(5)FeCO3在空气中灼烧可制得铁系氧化物材料。
①4Fe(s)+3O2(g)![]() 2Fe2O3 ΔH=﹣1648 kJ·mol-1
2Fe2O3 ΔH=﹣1648 kJ·mol-1
②C(s)+O2(g)![]() CO2(g) ΔH=﹣393 kJ·mol-1
CO2(g) ΔH=﹣393 kJ·mol-1
③2Fe(s)+2C(s)+3O2(g)![]() 2FeCO3(s) ΔH=﹣1480 kJ·mol-1
2FeCO3(s) ΔH=﹣1480 kJ·mol-1
根据盖斯定律,①+②×4-③×2得FeCO3在空气中灼烧生成Fe2O3的热化学方程式:4FeCO3(s)+ O2(g) = 2Fe2O3(s) + 4CO2(g) ΔH=﹣260 kJ·mol-1;(6)欲利用滤渣D为原料制取Al2O3,向滤渣D中加入适量NaOH溶液,过滤,向滤液中通入足量CO2,过滤并洗涤沉淀,加热所得沉淀至恒重,可得Al2O3。


科目:高中化学 来源: 题型:
【题目】下列有机反应:①甲烷与氯气光照反应 ②乙醛制乙酸 ③乙烯使溴水褪色 ④乙醇制乙烯 ⑤乙醛制乙醇 ⑥乙酸制乙酸乙酯 ⑦乙酸乙酯与NaOH溶液共热 ⑧液态植物油制人造脂肪 ⑨乙烯制乙醇的说法正确的是
A. ②⑤的反应类型相同 B. ⑥⑦的反应类型不同
C. ④与其他8个反应的类型都不同 D. ①③⑧属于同一种反应类型
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是()
3C+4D反应中,表示该反应速率最快的是()
A.v(A)=0.5 mol/(L·min) B.v(B)=0.3 mol/(L·min)
C.v(C)=0.8 mol/(L·min) D.v(D)=1 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中的氯离子浓度与50 mL 0.1 mol·L-1氯化铝溶液中氯离子的浓度相等的是( )
A.150 mL 0.1 mol·L-1 NaCl溶液
B.75 mL 0.2 mol·L-1 NH4Cl溶液
C.300 mL 0.1 mol·L-1 KCl溶液
D.150 mL 0.1 mol·L-1 FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A+3B![]() 2C。若维持温度和压强不变,当达到平衡时,容器容积为VL,其中C气体的体积占10 % ,下列推断正确的是( )
2C。若维持温度和压强不变,当达到平衡时,容器容积为VL,其中C气体的体积占10 % ,下列推断正确的是( )
①原混合气体的体积为1.2L
②原混合气体的体积为1.1L
③反应达到平衡时气体A消耗掉0.05VL
④反应达到平衡时气体B消耗掉0.05VL
A. ②③ B. ②④ C. ①③ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
A. H+、I-、Br2、Na+ B. Ag+、NO3-、Cl-、K+
C. K+、Ba2+、OH-、SO42- D. Cu2+、NH4+、Br-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是
A.向NaAlO2溶液中通入足量CO2,有白色沉淀产生,说明碳酸的酸性强于氢氧化铝
B.用铂丝蘸取某溶液进行焰色反应,火焰呈黄色,说明溶液中不含有K+
C.在KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去,说明SO2具有漂白性
D.向某FeCl2溶液中,加入Na2O2粉末出现红褐色沉淀,说明原FeCl2已氧化变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
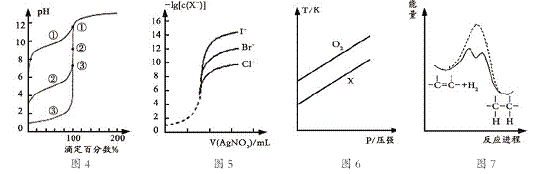
A. 用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由图4曲线确定①的酸性最强
B. 用0.0100mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/LCl-、Br-及I-的混合溶液,由图5曲线,可确定首先沉淀的是Cl-
C. 在体积相同的两个密闭容器中,分别充入相同质量O2和X气体,由图6可确定X可能是CH4气体
D. 由图7可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com