
 ij�����Һ�п��ܺ��е��������±���ʾ��
ij�����Һ�п��ܺ��е��������±���ʾ��| ���ܴ������е������� | H+��Ag+��Mg2+��Al3+��NH4+��Fe3+ |
| ���ܴ������е������� | Cl-��Br-��I-��CO32-��AlO2- |
| Cl2���������״���� | 11.2L | 22.4L | 28.0L |
| n��Cl-�� | 2.5mol | 3.5mol | 4.0mol |
| n��Br-�� | 3.0mol | 2.5mol | 2.0mol |
| n��I-�� | x mol | 0 | 0 |
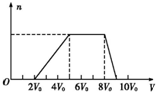
���� ��1���ٿ�ʼ����2V0��������˵�������ķ�Ӧ�ǣ�H++OH-�TH2O���ټ�������������Һ��5V0��ͼ�������֪���ɳ������������ӦΪAl3++3OH-�TAl��OH��3������������������Һ3V0�����������������ƣ����������䣬˵���������ƺ���Һ�е�笠����ӷ�Ӧ��NH4++OH-?NH3•H2O����������������Һ3V0��������������������Һ��������ʼ�ܽ⣬������9V0����������Һ������ȫ���ܽ⣬�����ķ�ӦΪAl��OH��3+OH-�TAlO2-+H2O��������������V0�����ݶ�����ϵ�����ж����Ӵ���������������ʵ���֮�ȣ�
�ڳ�����������ΪAl��OH��3����NaOH��Һ��
��2����ԭ�ԣ�I-��Br-����������11.2Lʱ����I-��Ӧ����Ӧ����Һ�л���I-xmol����˵��ͨ��11.2LCl2ֻ������Cl2+2I-�TI2+2Cl-��Br-û�з�Ӧ����ԭ��Һ��Br-Ϊ2.5mol���������������ʵ���������ɵ������ӵ����ʵ������������ԭ��Һ��Cl-�����ʵ�����
������11.2L���22.4L��Br-�����ʵ�����С��������Cl2 +2Br-�TBr2+2Cl-��Cl2+2I-�TI2+2Cl-������Br-�ı仯ֵ����μӷ�Ӧ���������������I-��Ӧ�����������ʵ������Լ�I-�����ʵ������������ʵ���֮�ȵ��ڼ�����֮��д������ʽ��
��� �⣺��1���ٸ���ͼ��ʼ����NaOHû�г����������������һ����H+�������ӹ����֪��һ��������CO32-��AlO2-��
��ʼ����2V0��������˵�������ķ�Ӧ�ǣ�H++OH-�TH2O�������г��������������ʧ����һ��û��Mg2+��Fe3+��Ag+����Al3+��
�ټ�������������Һ��5V0��ͼ�������֪���ɳ������������ӦΪAl3++3OH-�TAl��OH��3������������������Һ3V0��
���������������ƣ����������䣬˵���������ƺ���Һ�е�笠����ӷ�Ӧ��NH4++OH-?NH3•H2O����������������Һ3V0��
������������������Һ��������ʼ�ܽ⣬������9V0����������Һ������ȫ���ܽ⣬�����ķ�ӦΪAl��OH��3+OH-�TAlO2-+H2O��������������V0��
�������������䣬��ӦΪNH4++OH-?NH3•H2O�ķ�Ӧ������NH4+��
ͼ�з�Ӧ������ȷ���Ƿ�K+����������һ�������ڵ�������ΪMg2+��Fe3+��Ag+��һ�������ڵ���������CO32-��AlO2-��һ�����ڵ���������H+��NH4+��Al3+�����ʵ���֮��=2V0��3V0��V0=2��3��1��
�ʴ�Ϊ��Mg2+��Fe3+��Ag+��CO32-��AlO2-��H+��NH4+��Al3+Ϊ2��3��1��
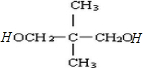
�ڳ�����������ΪAl��OH��3����NaOH��Һ����ƫ�����ƺ�ˮ����Ӧ�����ӷ���ʽΪAl��OH��3+OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
��2���ٵ�ͨ��Cl2�����Ϊ11.2 Lʱ����Һ��I-����ʣ�࣬������ֻ��I-��Ӧ��Cl2+2I-=I2+2Cl-������1mol Cl-��Cl-��ʼ���ʵ����ǣ�2.5-1��mol=1.5 mol��
�ɱ������ݿ�֪��Br-��ʼ���ʵ�����3 mol����ͨ��Cl2 22.4 L��1molʱ����������Br-���ʵ���Ϊ��n��Br-��=3.0 mol-2.5 mol=0.5 mol��
�ɷ�ӦCl2+2Br-=Br2+2Cl-��֪������n��Cl2��=$\frac{1}{2}$n��Br-��=0.25 mol��
����Cl2+2I-=I2+2Cl-�з�Ӧ���ĵ�Cl2Ϊ��1 mol-0.25 mol=0.75 mol�����ԭ��Һ�е�I-Ϊ��n��I-��=2��n��Cl2��=0.75 mol��2=1.5 mol��
��ͨ��Cl2 22.4 Lʱ���μӷ�Ӧ��Cl2��Br-��I-���ʵ���֮��Ϊ��1 mol��0.5 mol��1.5 mol=2��1��3=4��2��6�������ӷ���ʽΪ4Cl2+2Br-+6I-=8Cl-+Br2+3I2��
�ʴ�Ϊ��4Cl2+2Br-+6I-=8Cl-+Br2+3I2��
���ɢٷ�����֪��ԭ��Һ�е�Cl-��Br-��I-�����ʵ���Ũ��֮��Ϊ1.5mol��3mol��1.5mol=1��2��1���ʴ�Ϊ��1��2��1��
���� ���⿼�����ʺ����IJⶨ����Ŀ�漰���ӵ��жϺͼ��㡢ͼ�����ݷ����ķ����ͷ�Ӧʵ�ʣ���Ŀ�Ѷ��еȣ�ע��������ӵĻ�ԭ���Լ����������жϷ�Ӧ�ij̶ȣ���Ϸ���ʽ���㣬������ѧ���ķ����������飮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
�� ��
�� ��
�� ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
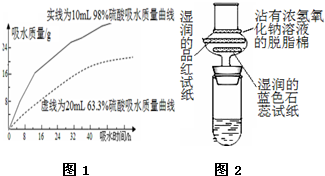 Ũ�����ڸ��л�ѧʵ�������ź���Ҫ������
Ũ�����ڸ��л�ѧʵ�������ź���Ҫ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������м���ŨH2SO4����ַ�������˵��Ũ���������ˮ�� | |
| B�� | Ũ���ᱣ������ɫ��ϸ��ƿ�У������ڵ��������� | |
| C�� | ��ζ����ȶ������ȷֽⶼ���ɰ��� | |
| D�� | ��Fe��NO3��2��Һ�еμ�ϡ���ᣬ�����Եı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
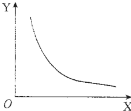
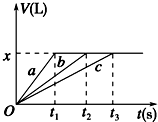 �������ʵ����Ľ���Na��Mg��Al�ֱ���100mL 2mol•L-1�����ᷴӦ��ʵ����������������V�����ۺ�Ϊ��״������ʱ��t�Ĺ�ϵ��ͼ��ʾ��������˵��������ǣ�������
�������ʵ����Ľ���Na��Mg��Al�ֱ���100mL 2mol•L-1�����ᷴӦ��ʵ����������������V�����ۺ�Ϊ��״������ʱ��t�Ĺ�ϵ��ͼ��ʾ��������˵��������ǣ�������| A�� | x=2.24 | B�� | �Ƶ����ʵ���Ϊ0.2 mol | ||
| C�� | ��Ӧʱ��Na��Mg��Al������ | D�� | ����bΪMg�����ᷴӦ��ͼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 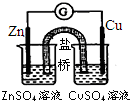 �����õ�����G����ָ���ƫת����ɱȽ�Zn��Cu�Ľ����������� | |
| B�� | 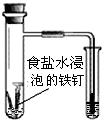 �����Ҳ�С�Թ���Һ��ı仯�������ж��������������ⸯʴ | |
| C�� | 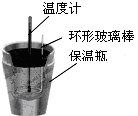 �ⶨ�к��� | |
| D�� | 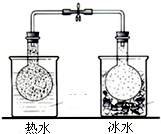 ��������ƿ��������ɫ�ı仯����ˮ�б����ˮ�б�dz�������ж�2NO2��g��?N2O4��g����һ�����ȷ�Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com