
| A. | 生石灰 | B. | 无水乙醇 | C. | 浓硫酸 | D. | 固体硝酸铵 |
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:实验题
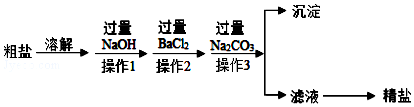
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 镀铜铁制品镀层受损后,铁制品不易生锈 | |
| C. | 加热0.1mol/LNa2CO3溶液,CO32-的水解程度和溶液的pH均增大 | |
| D. | 对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 | 实验结论 |
Ⅰ.取第一份溶液和适量稀盐酸加入下列装置的试管中,把澄清的石灰水加入烧杯中 | 导管口有气泡, | 证明含有CO32- |
| Ⅱ.取第二份溶液,先滴加稀盐酸后加 | 证明含有SO42- | |
| Ⅲ.取第三份溶液加入过量BaCl2溶液,过滤,除去SO42-和CO32-,再滴加AgNO3溶液和稀硝酸 | 有白色沉淀生成 | 证明含有Cl- |
| Ⅳ.取第四份溶液进行焰色反应 | 透过蓝色钴玻璃火焰呈紫色 | 证明含有K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |
| B. |
| C. |
| D. |
|
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 科学家根据元素的原子结构和性质,把它们科学有序地排列起来,得到了元素周期表 | |
| B. | 原子序数是按元素原子核电荷数递增的顺序给元素编的号 | |
| C. | 元素周期表上对金属元素、非金属元素用不同的颜色做了区分 | |
| D. | 元素周期表共有7个周期,18个族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
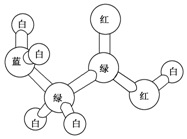 某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )
某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )| A. | 卤代羧酸 | B. | 酯 | C. | 氨基酸 | D. | 乙醇钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
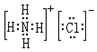 ,其中存在的化学键类型为离子键和共价键.
,其中存在的化学键类型为离子键和共价键.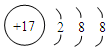 ;元素D最高价氧化物的水化物的化学式为H3PO4或HPO3.
;元素D最高价氧化物的水化物的化学式为H3PO4或HPO3.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
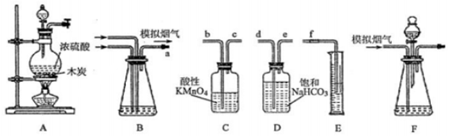
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com