
分析 (1)实验①中用去n(NaOH)=100 mL×(2.0 mol•L-1-1.0 mol•L-1)=0.1 mol
无论是Al还是Al2O3,与NaOH溶液反应后都生成NaAlO2,铝热剂中
n(Al)=n(NaOH)×2=0.2 mol;
实验②所得溶液中,根据“电荷守恒”有n(H+)+2×n(Fe2+)+3×n(Al3+)=n(Cl-)
则n(Fe2+)=$\frac{{140mL×4.0mol•{L^{-1}}-140mL×1.0mol•{L^{-1}}-3×0.1mol}}{2}$=0.06 mol
铝热剂中n(Fe2O3)=n(Fe2+)×$\frac{1}{2}$×2=0.06 mol;
根据m=nM计算Al、氧化铁的质量;
(2)根据上述计算结果,②的铝热剂中有0.1molAl、0.03molFe2O3,根据反应2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3知,氧化铁完全反应消耗0.06molAl,所以还剩余0.04molAl,同时生成0.06molFe和0.03mol氧化铝,
根据转移电子相等计算生成氢气体积.
解答 解:(1)实验①中用去n(NaOH)=100 mL×(2.0 mol•L-1-1.0 mol•L-1)=0.1 mol
无论是Al还是Al2O3,与NaOH溶液反应后都生成NaAlO2,铝热剂中
n(Al)=n(NaOH)×2=0.2 mol,m(Al)=0.2mol×27g/mol=5.4 g;
实验②所得溶液中,根据“电荷守恒”有n(H+)+2×n(Fe2+)+3×n(Al3+)=n(Cl-)
则n(Fe2+)=$\frac{{140mL×4.0mol•{L^{-1}}-140mL×1.0mol•{L^{-1}}-3×0.1mol}}{2}$=0.06 mol
铝热剂中n(Fe2O3)=n(Fe2+)×$\frac{1}{2}$×2=0.06 mol,m(Fe2O3)=0.06mol×160g/mol=9.6 g,
答:这包铝热剂中铝的质量和氧化铁的质量分别是5.4g、9.6g;
(2)根据上述计算结果,②的铝热剂中有0.1molAl、0.03molFe2O3,根据反应2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3知,氧化铁完全反应消耗0.06molAl,所以还剩余0.04molAl,同时生成0.06molFe和0.03mol氧化铝,
根据转移电子相等计算生成氢气体积,所以实验②中所得H2在标准状况下体积为V(H2)=n(H2)×22.4 L•mol-1=[n(Al)×$\frac{3}{2}$+n(Fe)]×22.4 L•mol-1=(0.04mol×$\frac{3}{2}$+0.06mol)×22.4L/mol=2.688 L,
答:实验②产生气体的体积(标准状况)为2.688L.
点评 本题考查混合物的有关计算,为高频考点,侧重考查学生分析计算能力,明确物质的性质及物质之间的反应是解本题关键,注意每一份为总混合物的一半,(1)题易漏掉另一半的铝热剂质量,(2)题易计算所有铝热剂与稀盐酸反应生成氢气体积,为易错题.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:选择题
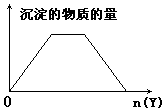
| A. | 向NaOH和Ca(OH)2的混合液中通入CO2 | |
| B. | 向HCl和AlCl3的混合液中滴加NaOH | |
| C. | 向NH4Cl和AlCl3的混合液中滴加NaOH | |
| D. | 向含NaOH的NaAlO2溶液中滴加盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
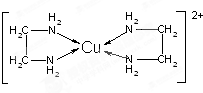 铜是过渡金属元素,可以形成多种化合物.
铜是过渡金属元素,可以形成多种化合物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 5.2 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KAl(SO4)2═K++Al3++SO42- | B. | NaH2PO4═Na++H2PO4- | ||
| C. | H2S?2H++S2- | D. | NaClO═Na++Cl-+O2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com