
【题目】2018年6月27日,国务院发布《打赢蓝天保卫战三年行动计划》,该计划是中国政府部署的一项污染防治行动计划,旨在持续改善空气质量,为群众留住更多蓝天。对废气的进行必要的处理,让空气更加清洁是环境科学的重要课题。
(1)已知:N2(g)+O2(g)=2NO(g) △H1=+180.5kJ/mol
C (s)+O2(g)=CO2(g) △H2=-393.5kJ/mol
2C (s)+O2(g)=2CO(g) △H3=-221.0kJ/mol
若某反应的平衡常数表达式为![]() ,请写出此反应的热化学方程式_________________。
,请写出此反应的热化学方程式_________________。
(2)用如图所示的电解装置可将雾霾中的NO、SO2分别转化为NH![]() 和SO
和SO![]()
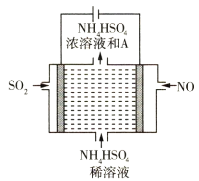
①写出物质A的化学式____________。
②NO在电极上发生的反应为 _________________。
SO2在电极上发生的反应为 __________________。
(3)工业上常用氨水吸收SO2,可生成NH4HSO3和(NH4)2SO3。
①某同学测得氨水吸收SO2所得溶液中NH4HSO3和(NH4)2SO3的物质的量之比恰好为2:1,写出该吸收过程的总反应方程式______________________________________。
②已知常温下H2S的电离常数Ka1=1.3×10-7,Ka2=7.1×10-15,将等物质的量浓度的NaHS与Na2S溶液等体积混合,所得溶液中离子浓度大小顺序为__________________。(用物质的量浓度符号由大到小排列)
【答案】2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H3=-746.5kJ/mol H2SO4 2NO+12H++10e-=2NH4++2H2O 5SO2+10H2O-10e-=5SO42-+20H+ 3SO2+4NH3·H2O=2NH4HSO3+(NH4)2SO3+H2O c(Na+)>c(HS-)>c(S2-)>c(OH-)>c(H+)
N2(g)+2CO2(g) △H3=-746.5kJ/mol H2SO4 2NO+12H++10e-=2NH4++2H2O 5SO2+10H2O-10e-=5SO42-+20H+ 3SO2+4NH3·H2O=2NH4HSO3+(NH4)2SO3+H2O c(Na+)>c(HS-)>c(S2-)>c(OH-)>c(H+)
【解析】
(1) 平衡常数表达式为![]() ,反应物为NO、CO,生成物为N2、CO2;根据盖斯定律,求解即可;
,反应物为NO、CO,生成物为N2、CO2;根据盖斯定律,求解即可;
(2)①SO2、NO分别变为铵根离子和硫酸根离子,则A为硫酸;
②NO在电极上失电子,变为铵根离子;SO2失电子,与水反应生成硫酸根离子和氢离子;
(3)①NH4HSO3和(NH4)2SO3的物质的量之比恰好为2:1,根据硫原子、氮原子守恒,则需要二氧化硫的系数为3,氨气为4;
②根据电离平衡常数,求解NaHS的水解平衡常数,可确定NaHS的水解程度大于电离程度,而Na2S只水解生成HS-,即可判断溶液中的离子浓度关系;
(1) 平衡常数表达式为![]() ,反应物为NO、CO,生成物为N2、CO2;①N2(g)+O2(g)=2NO(g) △H1=+180.5kJ/mol;②C(s)+O2(g)=CO2(g) △H2=-393.5kJ/mol;③2C(s)+O2(g)=2CO(g) △H3=-221.0kJ/mol,根据盖斯定律,2②-①-③可得2CO(g)+ 2NO(g)= N2(g)+CO2(g) △H=-746.5kJ/mol;
,反应物为NO、CO,生成物为N2、CO2;①N2(g)+O2(g)=2NO(g) △H1=+180.5kJ/mol;②C(s)+O2(g)=CO2(g) △H2=-393.5kJ/mol;③2C(s)+O2(g)=2CO(g) △H3=-221.0kJ/mol,根据盖斯定律,2②-①-③可得2CO(g)+ 2NO(g)= N2(g)+CO2(g) △H=-746.5kJ/mol;
(2)①SO2、NO分别变为铵根离子和硫酸根离子,则A为硫酸,其化学式为:H2SO4;
②NO在电极上失电子,变为铵根离子,发生的反应为2NO+12H++10e-=2NH4++2H2O;SO2失电子,与水反应生成硫酸根离子和氢离子,电极反应式为:5SO2+10H2O-10e-=5SO42-+20H+;
(3)①NH4HSO3和(NH4)2SO3的物质的量之比恰好为2:1,根据硫原子、氮原子守恒,则需要二氧化硫的系数为3,氨气为4,则方程式为:3SO2+4NH3·H2O=2NH4HSO3+(NH4)2SO3+H2O;
②HS-的水解平衡常数Kw/ Ka1=![]() ,S2-的一级水解常数(一级水解远远大于二级水解)为Kw/ Ka2=
,S2-的一级水解常数(一级水解远远大于二级水解)为Kw/ Ka2=![]() ,显然HS-的水解程度大于其电离程度,但是小于S2-的水解程度,而S2-只水解,且水解程度大于HS-的水解程度和电离程度,则溶液中的离子浓度为c(Na+)>c(HS-)>c(S2-);水解溶液呈碱性,且为少量水解,则c(S2-)>c(OH-)>c(H+),答案为:c(Na+)>c(HS-)>c(S2-)>c(OH/span>-)>c(H+)。
,显然HS-的水解程度大于其电离程度,但是小于S2-的水解程度,而S2-只水解,且水解程度大于HS-的水解程度和电离程度,则溶液中的离子浓度为c(Na+)>c(HS-)>c(S2-);水解溶液呈碱性,且为少量水解,则c(S2-)>c(OH-)>c(H+),答案为:c(Na+)>c(HS-)>c(S2-)>c(OH/span>-)>c(H+)。


科目:高中化学 来源: 题型:
【题目】硝酸工业尾气中氮的氧化物NO、NO2被氢氧化钠溶液吸收的主要反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O,现有aL(标准状况)NO和NO2混合气体被足量氢氧化钠溶液吸收,没有气体残余,下列说法不正确的是 ( )
A.实际参加反应的氢氧化钠的物质的量是a/22.4 mol
B.混合气体气体中NO2体积一定大于(等于)NO体积
C.溶液中NaNO3物质的量一定小于(等于)NaNO2物质的量
D.若生成的NaNO2与NaNO3的物质的量之比为3:1,则混合气体中NO与NO2的体积比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量的铜片与![]() 浓硫酸加热充分反应,收集到标准状况下的
浓硫酸加热充分反应,收集到标准状况下的![]() 气体VL,下列对此反应的有关说法中错误的是
气体VL,下列对此反应的有关说法中错误的是 ![]()
A. 该反应体现了浓硫酸的酸性和强氧化性
B. 反应结束后两种反应物均有剩余
C. 被还原的硫酸为![]()
D. 参加反应的Cu为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼(BN)晶体有多种结构,六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,有白色石墨之称,具有电绝缘性,可作高温润滑剂。立方相氮化硼是超硬材料,硬度可媲美钻石,常被用作磨料和刀具材料。它们的晶体结构如图所示,关于两种晶体的说法,错误的是
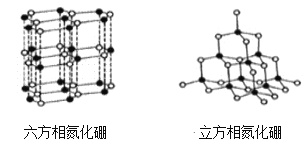
A. 六方相氮化硼属于混合晶体,其层间是靠范德华力维系,所以质地软
B. 立方相氮化硼含有σ键和π键,所以硬度大
C. 六方氮化硼不能导电是因为其层结构中没有自由电子
D. 相同质量的六方相氮化硼和立方相氮化硼所含共价键数不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,3种物质的电离平衡常数如下表:
物质 | HCOOH | CH3COOH | NH3·H2O |
电离平衡常数K | 1.77×104 | 1.75×105 | 1.76×105 |
下列说法不正确的是
A.等物质的量浓度时,溶液pH:HCOONa<CH3COONa
B.pH均为3时,溶液浓度:c(HCOOH)>c(CH3COOH)
C.HCOOH溶液与氨水混合,当溶液pH=7时,c(HCOO-)=c(NH4+)
D.等物质的量浓度等体积的CH3COOH溶液和氨水混合,溶液pH约为7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学探究SO2与Fe3+盐溶液的反应,进行了如下实验:已知:Fe3++HSO3-Fe(HSO3)2+(红棕色)
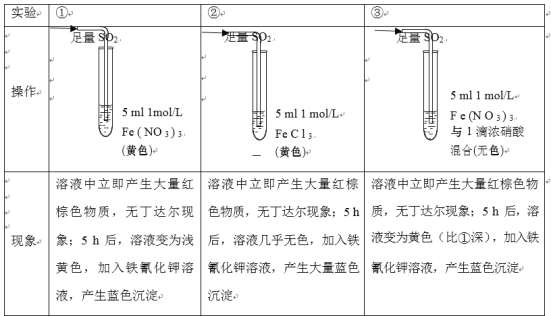
结合上述实验,下列说法不正确的是
A.产生红棕色物质的反应速率快于SO2与Fe3+氧化还原反应的速率
B.①与②对照,说明阴离子种类对SO2与Fe3+氧化还原反应的速率有影响
C.Fe(NO3)3溶液中加入1滴浓硝酸后变为无色,说明浓硝酸具有漂白性
D.5h后③比①黄色更深不能证明是NO3-浓度的增大减慢了SO2与Fe3+反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物K是一种化工原料,其合成路线如下:
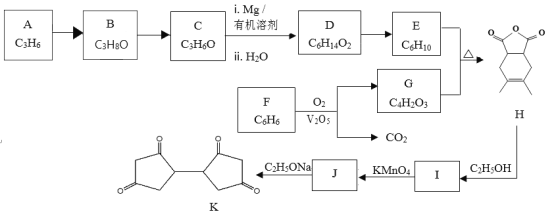
已知:i: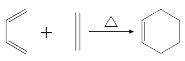
ii: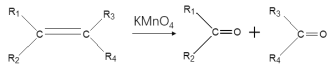
iii: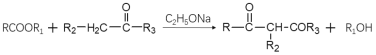 (R1为烃基)
(R1为烃基)
(1)按照官能团分类,A的类别是_______________________。
(2)C分子中只有一种类型的氢原子,B→C的化学方程式是_____________________。
(3)已知D的核磁共振氢谱有2个峰,1molD与足量Na反应可生成1molH2,写出D→E的化学方程式是 ___________________________ 。
(4)G的结构简式是___________________________。
(5)由F制备G,产物G与CO2物质的量之比为___________________________。
(6)M是G的同分异构体,写出符合下列条件的M的结构简式_________________。
a.能与NaHCO3反应产生气泡
b.能发生银镜反应
(7)写出结构简式:I _____________、J _________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,下列实验用如图所示装置不能完成的是

A.测定一定质量的Cu和Mg混合物中Cu的含量
B.确定分子式为C2H6O的有机物分子中含活泼氢原子的个数
C.比较Fe3+和Cu2+对一定质量的双氧水分解反应的催化效率
D.测定一定质量的Na2SO4·xH2O晶体中结晶水数目
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com