
| A��һ������Clһ |
| B��һ������A13+��NH4+ |
| C��һ��������Mg2+�����ܴ���A13+ |
| D����Һ��SO42�D��Ũ����0. 3 mol/L |
 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������,��1 L pH=12�İ�ˮ��ˮϡ��Ϊ10 L����Һ��pH=11 |
| B���мס�����������Һ,��ü�pH=a,�ҵ�pH=a+1,�������к͵����ʵ���Ũ�ȵ������NaOH��Һ,��ס�����������V (��)>10V(��) |
C����Ũ�Ⱦ�Ϊ0.1 mol��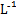 ��MgCl2��CuCl2�����Һ����μ��백ˮ,��������ɫ����,˵��Ksp[Cu(OH)2]>Ksp[Mg(OH)2] ��MgCl2��CuCl2�����Һ����μ��백ˮ,��������ɫ����,˵��Ksp[Cu(OH)2]>Ksp[Mg(OH)2] |
| D��ˮ�����ӻ�����KW�����¶ȵ����߶�����,˵��ˮ�ĵ����Ƿ��ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ʹ��̪��Һ������Һ�� Na+��Cl����SO42����Fe3�� |
| B��ˮ������Һ�У�K����SO42����Cl����H�� |
| C������Al��Ӧ�ų���������Һ�У�Na����Ca2����Cl����HCO3�� |
| D��ʹʯ���������Һ�У�Ba2����Na����AlO2����Cl�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Fe3����Cl����NO3�� | B��Na����HCO3����SO42- |
| C��Ag����NH4����NO3�� | D��Na����SO32-��SO42�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��K+��MnO4����Na+��Cl�� | B��K+��Na+��NO3����CO32�� |
| C��Na+��H+��NO3����SO42�� | D��Fe3+��Na+��Cl����SO42�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 H+ + A2����������˵����ȷ����( )
H+ + A2����������˵����ȷ����( )�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 H+ +A2����
H+ +A2����| A��c(Na+)>c(A2��)>c(OH��)>c(HA��)>c(H+) |
| B��c(Na+)> c(OH��)>c(HA��)> >c(A2��) > c(H+) |
| C��c(Na+)> c(H+)> c(A2��)> c(OH��)>c(HA��) |
| D��c(A2��)>c(Na+)> c(OH��) > c(H+)>c(HA��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��pH��0����Һ�У�Na����[Al(OH)4]����K+��NH4+ |
| B����ˮ�������c(H��)��10��12mol/L����Һ�У�C1-��HCO3-��NH4+��SO32- |
| C�������������H2����Һ�У�Mg2+��NH4+��C1-��SO42- |
| D���μ�ʯ����Һ����ɫ����Һ��K+��Ba2+��NO3-��OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Ư�ۺ�����������������ˮ�Ĵ��������ߵ�����ԭ������ͬ�� |
| B��SO32����ClO����NO3�����������������Һ���ܴ������� |
| C�������ô��������IJ���ƿ����ʽ�ζ���ʢȡ��Һ�����ߵ�ԭ������ͬ�� |
| D��98%��Ũ�����õ������ˮϡ�ͺ��������������Ϊ49% |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com