
【题目】下列物质的转化在给定条件下均能通过一步反应实现的是( )
A. NaAlO2(aq)![]() AlCl3
AlCl3![]() Al2O3 B. N2
Al2O3 B. N2![]() NO2
NO2![]() HNO3
HNO3
C. NaCl(饱和)![]() NaHCO3
NaHCO3![]() Na2CO3 D. FeS2
Na2CO3 D. FeS2![]() SO3
SO3![]() H2SO4
H2SO4
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法正确的是( )

A. 加热时,①中上部汇集了NH4Cl固体
B. 加热时,②中溶液变红,冷却后又都变为无色
C. 加热时,③中溶液红色褪去,冷却后溶液变红,体现SO2的漂白性
D. 三个“封管实验”中所发生的化学反应都是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制取物质、探究物质的性质是学习化学必备的素养之一。
回答下列问题。
(1)实验室从含碘废液(除水外含CCl4、I2、I-等)中回收碘,其实验流程如下。

回答下列问题:
①物质X的名称为________;
②操作Ⅰ选用的装置为______(填标号);

③含碘废液中加入稍过量的Na2SO3溶液将I2还原为I-,反应的离子方程式为___。
④氧化剂Y可用Cl2,也可以用H2O2。将同物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为________。
(2)某研究小组查阅资料知:氧化性的强弱顺序为:Cl2>IO3->I2。用如图装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色。

①NaOH溶液的作用是______,反应的离子方程式为___________。
②溶液由黄色最后变为无色所发生反应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质按照碱、酸、盐顺序正确组合的是()
A.Na2CO3 H2SO4 NaHCO3B.NaOH HCl NaCl
C.CH3COOH NaOH CaCl2D.KOH CaCO3 HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班同学用如下实验探究过氧化氢的性质。回答下列问题:
(1)甲组同学拟配制5%的H2O2溶液,他们先从文献查得H2O2的稳定性与pH的关系如图所示。则配制H2O2溶液时应滴入几滴_____________(填“稀硫酸”或“氨水”)。

(2)乙组同学向一支试管中加入2mLFeCl2溶液,再滴入几滴甲组同学配制的H2O2溶液,最后滴人KSCN溶液,溶液变红,H2O2与Fe2+发生反应的离子方程式为_________________;另取一支试管,向其中加入SO2与BaCl2混合溶液2mL,再滴入几滴5%的H2O2溶液,现象是_____________。
(3)丙组同学取2mLKMnO4溶液于试管中,向其中滴几滴5%的H2O2溶液,发现溶液逐渐褪色,该反应中的还原剂是____________(填化学式)。
(4)丁组同学向一支试管中加入2mL5%的H2O2溶液、0.5mL乙醚、1mLlmol/LH2SO4溶液和3~4滴0.5mol/LK2Cr2O7溶液,发现上层乙醚层为蓝色(CrO5的乙醚溶液),一段时间后上层蓝色消失。

①乙醚的主要作用是____________。
②开始时,H2O2溶液与K2Cr2O7酸性溶液反应生成CrO5,该反应属于____________(填“氧化还原”或“非氧化还原”)反应。
③一段时间后,乙醚层中的CrO5与水相中的H+作用生成Cr3+并产生无色气泡,从而使蓝色逐渐消失,该反应的离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,萘可以被硝硫混酸硝化生成二硝基物,它是1.5﹣二硝基萘( 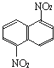 )和1.8﹣二硝基萘(
)和1.8﹣二硝基萘( 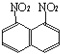 )的混合物.后者可溶于质量分数大于98%的硫酸,而前者不能.利用这个性质可以将这两种异构体分离.将上述硝化产物放入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1.8﹣二硝基萘,应彩的方法是( )
)的混合物.后者可溶于质量分数大于98%的硫酸,而前者不能.利用这个性质可以将这两种异构体分离.将上述硝化产物放入适量的98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中得到固体1.8﹣二硝基萘,应彩的方法是( )
A.蒸发浓缩结晶
B.向滤液中加入水后过滤
C.用Na2CO3溶液处理滤液
D.将滤液缓缓加入水中过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 投入铁片产生H2的溶液中可大量存在H+、Mg2+、SO![]() 、NO
、NO![]()
B. 将过量二氧化硫气体入冷氨水中:SO2+NH3·H2O===HSO![]() +NH
+NH![]()
C. 用酒精萃取碘水中的碘,水从分液漏斗下口放出,碘的酒精溶液从分液漏斗上口倒出
D. 高炉炼铁原理是用一氧化碳还原四氧化三铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对新制氯水与久置氯水性质的叙述正确的是( )
A. 都为黄绿色 B. 都具有漂白性
C. 都能与硝酸银溶液产生白色沉淀 D. 都能使紫色石蕊试液呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备Fe3O4纳米材料的流程示意图如下:


已知:步骤⑤中,相同条件下测得Fe3O4的产率与R( )的关系如图所示。
)的关系如图所示。
(1)为提高步骤①的反应速率,可采取的措施是_______________(任写一点) 。
(2)步骤②中,主要反应的离子方程式是________________________。
(3)浊液D中铁元素以FeOOH形式存在。步骤④中,反应的化学方程式是___________________;步骤④中,反应完成后需再加热一段时间除去剩余H2O2目的是____________________________
(4)⑤反应的离子方程式为_________________ ;步骤⑤中的“分离”包含的步骤有______________________。
(5)设浊液D中FeOOH的物质的量为amol,滤液B中的铁元素的物质的量为bmol。为使Fe3O4的产率最高,则![]() =_________。(填数值,小数点后保留3位)
=_________。(填数值,小数点后保留3位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com