
【题目】向浓度相等、体积均为50 mL 的 A、B 两份NaOH 溶液中,分别通入一定量的CO2后,再稀释到100 mL。
(1)在 NaOH 溶液中通入一定量的 CO2 后,溶液中溶质的可能组成是
①_________, ②________, ③________, ④________。
(2)在稀释后的溶液中逐滴加入0.2 mol/L 的盐酸,产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。
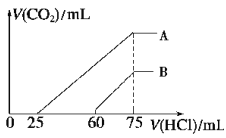
①A 曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生 CO2 的最大体积是_____mL(标准状况)。
②B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________。
③原 NaOH 溶液的物质的量浓度为________________。
【答案】(共10分)(1)①NaOH、Na2CO3(1分)②Na2CO3(1分)
③Na2CO3、NaHCO3(1分)④NaHCO3(1分)
(2)①224(2分)②NaOH、Na2CO3(2分)③0.3mol/L(2分)
【解析】
试题分析:(1)由CO2+2NaOH═Na2CO3+H2O、CO2+NaOH═NaHCO3,二氧化碳少量时固体为①Na2CO3和NaOH;以1:2恰好反应时为②Na2CO3;物质的量比介于1:1~1:2之间为③Na2CO3和NaHCO3;二氧化碳过量时为④NaHCO3;
(2)由图可知,对应B溶液来说,滴加盐酸60mL时没有气体生成,可能发生OH-+H+=H2O和CO32-+H+=HCO3-,假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积60mL远远大于碳酸氢钠生成氯化钠需要盐酸的体积(75-60)mL=15mL,说明原溶液中的溶质是NaOH和Na2CO3;
对于A溶液来说,滴加盐酸25mL时没有气体生成,可能发生OH-+H+=H2O和CO32-+H+=HCO3-,假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积25mL小于碳酸氢钠生成氯化钠需要盐酸的体积(75-25)mL=50mL,说明原溶液中的溶质是Na2CO3和NaHCO3,
①对于A溶液来说,滴加盐酸25mL时有气体生成,逐滴加入0.2molL-1 的盐酸,当生成CO2气体时,发生反应HCO3-+H+=H2O+CO2↑,
则HCO3-+H+=H2O+CO2↑
1 1
n(CO2)=0.05L×0.2mol/L=0.01mol,标况下体积为0.01mol×22.4L/mol=0.224L=224mL;
②由上述分析可知,B中溶质是Na2CO3和NaOH,由消耗盐酸的关系可知,物质的量比为3:1;
③加入足量的盐酸后的溶液中均只存在NaCl,n(HCl)=n(NaOH)=0.075L×0.2mol/L=0.015mol,c(NaOH)=n/V=0.015mol÷0.05L=0.3mol/L。


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
【题目】下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是( )
①NaHCO3②Al2O3③Al(OH)3 ④Al.
A.③④
B.②③④
C.①③④
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,水的离子积为1×10-12,若该温度下某溶液中的H+ 浓度为1×10-7mol/L则该溶液是
A.酸性 B.碱性 C.中性 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,将NO2装入带活塞的密闭容器中,当反应2NO2(g)![]() N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是( )
N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是( )
A.若体积减小一半,压强增大,V正增大,V逆减小
B.平衡向右移动,混合气体颜色一定会变浅
C.若体积减小一半,压强增大,但小于原来的两倍
D.平衡向右移动,混合气体的平均相对分子量减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是( )
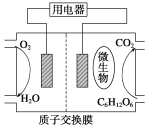
A.该电池能够在高温下工作
B.电池的负极反应式为C6H12O6+6H2O-24e-===6CO2↑+24H+
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体![]() L
L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaNO2是一种食品添加剂,它能致癌。酸性 KMnO4溶液与 NaNO2。的反应方程式是MnO4-+NO2-+□→Mn2++NO3-+H2O。下列叙述中正确的是( )
A.该反应中 NO2被还原 B.反应过程中溶液的pH 减小
C.生成1 mol NaNO3需消耗 0.4mol KMnO4 D.□中的粒子是 OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒。某兴趣小组进行下面实验探究,查阅资料知道:
①HNO2为弱酸,
②2NO+Na2O2=2NaNO2,
③2NO2+Na2O2=2NaNO3
④酸性KMnO4溶液可将NO和NO2-均氧化为NO3-,MnO4-还原成Mn2+。
NaNO2的制备方法可有如下2种方法(夹持装置和加热装置已略,气密性已检验):
制备装置1:
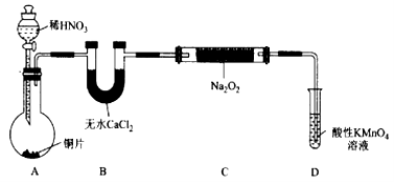
制备装置2:
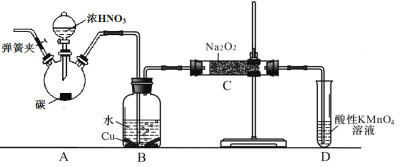
(1)在制备装置1中:
① 如果没有B装置,C中发生的副反应有 ;
② 甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质;于是在A装置与B装置间增加了 装置,改进后提高了NaNO2的纯度;
③ D装置发生反应的离子方程式为 。
(2)在制备装置2中:
① B装置的作用是 ;
② 写出装置A烧瓶中发生反应的化学方程式并用单线桥标出电子的转移 ;
③ 为避免B中逸出的气体中混有的杂质气体与Na2O2反应,应在B、C装置间增加一个装置,则该装置中盛放的药品名称为 ;
④ 实验经改进后可制得较纯亚硝酸钠,下列关于亚硝酸钠的说法正确的是________。
a.亚硝酸钠有咸味,可代替食盐食用
b.常温下,0.1mol/L亚硝酸钠溶液pH>1
c.0.1mol/L亚硝酸钠溶液中存在:c(Na+)+c(H+)=c(NO2-)+c(OH-)
d.0.1mol/L亚硝酸钠溶液中存在:c(NO2-)>c(Na+)>c(OH-)>c(H+)
⑤ 试设计实验检验装置C中NaNO2的存在(写出操作、现象和结论) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com