
| A. | 由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-=Al3+ | |
| B. | 由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+3OHˉ=Al(OH)3 | |
| C. | 由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Fe-2e-=Fe2+ | |
| D. | 由Fe、Cu、浓硝酸组成的原电池,开始时其负极反应式为:Cu-2e-=Cu2+ |
分析 A.原电池放电时,铝易失去电子而作负极;
B.原电池中,失电子发生氧化反应的电极是负极,该原电池中,铝和氢氧化钠反应而失去电子,则铝作负极;
C.原电池中,负极上失电子发生氧化反应,该原电池中,铁易失去电子而作负极;
D.Al、Cu、浓硝酸组成的原电池中,铝和浓硝酸发生钝化现象,铜和浓硝酸发生反应而失去电子,则铜作负极,用此电极电解硝酸银时,根据转移电子数相等计算消耗铜的质量.
解答 解:A.该原电池中,铝易失去电子而作负极,负极反应式为:Al-3e-=Al3+,放电时,故A正确;
B、由Mg、Al、NaOH溶液组成原电池,铝和氢氧化钠反应易失去电子而作负极,镁作正极,其负极反应式为:Al-3e-+4OH-═AlO2-+2H2O,故B错误;
C.该原电池中,铁易失去电子而作负极,铜作正极,其负极反应式为:Fe-2e-═Fe2+,故C正确;
D、Al、Cu、浓硝酸组成原电池作电源,铜作负极,负极反应式为:Cu-2e-=Cu2+,故D正确;
故选B.
点评 本题考查了原电池原理,易错选项是B和D,注意不能根据金属的活泼性确定原电池的正负极,要根据电极反应类型判断原电池的正负极,为易错点.


科目:高中化学 来源: 题型:解答题
 如表为元素周期表短周期的一部分.回答下列问题:
如表为元素周期表短周期的一部分.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
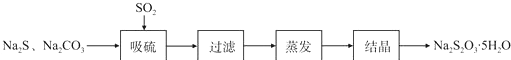
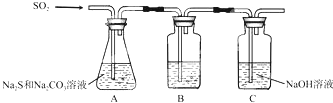
| 序号 | 实验操作 | 预期现象 | 结论 |
| ① | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解 滴加足量稀硝酸,再滴加少量AgNO3溶液,振荡 | 有白色沉淀生成 | 样品含NaCl |
| ② | 取少量样品于试管中,加入适量蒸馏水,充分振荡溶解 加入过量BaCl2溶液,搅拌,静置,用pH计测定上层清液pH | 有白色沉淀生成,上层清液pH大于9.6 | 样品含NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5730×3年 | B. | 5730×4年 | C. | 5730×6年 | D. | 5730×8年 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
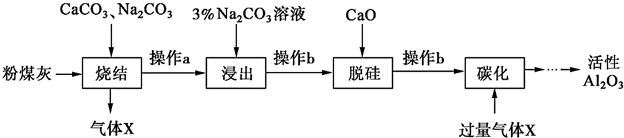
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
. 按1:1恰好反应生成两种酸性有机物,则另一种有机物的名称为乙酸.
按1:1恰好反应生成两种酸性有机物,则另一种有机物的名称为乙酸. .试剂c最好选用C(填字母序号).
.试剂c最好选用C(填字母序号). .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有机化合物都是从有机体中提炼出来的 | |
| B. | 有机物和无机物的性质完全不同 | |
| C. | 所有有机物均含有碳元素 | |
| D. | 所有有机物均含有氢元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com