
【题目】金属的冶炼方法有很多,有加热法,热还原法、 电解法、湿法冶金等:我国古代利用铁和硫酸铜溶液反应炼铜,属于___(填冶炼的方法);铝热反应是铝与一些金属氧化物在高温下反应,属于___(填冶炼的方法);写出铝与四氧化三铁的反应方程式:____。
科目:高中化学 来源: 题型:
【题目】锂/氟化碳电池稳定性很高。电解质为LiClO4的乙二醇二甲醚溶液,总反应为xLi+CFx=xLiF+C,放电产物LiF沉积在正极,工作原理如图所示。下列说法正确的是

A.正极的电极反应式为CFx+xe-+xLi+=xLiF+C
B.交换膜为阴离子交换膜
C.电解质溶液可用LiClO4的乙醇溶液代替
D.b极电势高于a极电势
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用以下装置探究氯气与氨之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨反应的装置。
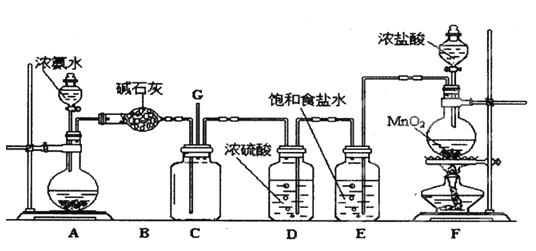
请回答下列问题:
(1)装置F中发生反应的化学方程式为____________________________.
(2)装置B中仪器的名称是___________;装置E的作用是______________________.
(3)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。写出反应的化学方程式___________________________________.
(4)装置C内当有a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗数常数为_______mol-1(用含a、b的代数式表示)。
(5)将用F、E、D装置制得的氯气通人含74gCa(OH)2的石灰乳中,最多可制得漂白粉_______g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置______。![]() 的中子数为________。
的中子数为________。
已知:P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;由此推知,其中最稳定的磷单质是________。
(2)氮和磷氢化物性质的比较:热稳定性:NH3________PH3(填“>”或“<”)。沸点:N2H4________P2H4(填“>”或“<”),判断依据是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工艺的一个重要工序是铜洗,其目的是用铜液(醋酸二氨合铜、氨水)吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应方程式为:Cu(NH3)2Ac+CO+NH3![]() [Cu(NH3)3CO]Ac (Ac-为CH3COO-的简写)
[Cu(NH3)3CO]Ac (Ac-为CH3COO-的简写)
(1)基态原子中未成对电子数最多的短周期元素X,与上述反应中所有元素均不在同一周期,该基态原子的电子排布式为________。
(2) [Cu(NH3)3CO]Ac组成元素中,第一电离能最大的元素是________。(填元素符号)。
(3)HAc可通过将CH3CHO氧化得到,比较HAc与乙醛的沸点高低,并说明原因:________________。
(4)C、N两种原子可形气体分子 (CN)2,也可形成有剧毒性的CN-。(CN)2性质与卤素单质类似,判断(CN)2中C原子轨道杂化类型为________。与CN-互为等电子体的一种非极性分子的化学式为________。
(5)铜晶胞结构如图,铜晶体中每个铜原子周围距离最近的铜原子数目为________。
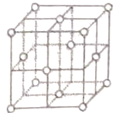 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室里制取少量FeCl3,可按照一定顺序连接下图中所列装置,所通过的气体过量且反应充分。试回答以下问题:
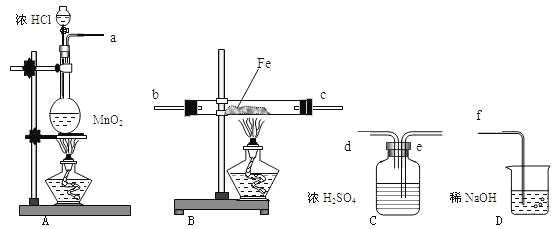
(1)实验时,各装置接口的连接顺序为___________________________(用a、b、c、d等字母表示);
(2)C装置的作用是________________________;
(3)D装置的作用是_____________________________________;
(4)检验B装置中反应后铁是否有剩余的方法是:_______________________;
(5)用此方法可制得无水氯化铁。你认为能否改用Fe和盐酸反应,再通入过量氯气、蒸干溶液的方法来制取无水氯化铁,________(答:是或否);说明理由:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色胶状沉淀,I为红褐色沉淀。(此转化关系中所用的试剂都是足量的)

(1)写出下列物质的化学式:F____________,G________________。
(2)将混合物中两种金属分离开的最简单的方法是___________。
(3)D→E的转化中,加入过量的X可能是_____________________。
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:______________________________________________;
H→I:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值。下列说法正确的是
A.2C+SiO2![]() 2CO↑十Si,则每生成4.48 L CO时转移电子0.4NA
2CO↑十Si,则每生成4.48 L CO时转移电子0.4NA
B.1 mol NH3完全溶于水,则n(NH3·H2O)+n(NH4+)=l mol
C.氯化铝在气态时以双聚分子存在,其球棍模型为![]() ,则1 mol双聚分子中含有电子数为128NA
,则1 mol双聚分子中含有电子数为128NA
D.2SO2(g)+O2(g)2SO3(l) △H=-a kJ·mol-1(a>0),则每生成2 mol SO3(l)时吸热a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3是一种用途比较广泛的盐。
(1)印刷电路板是由高分子材料和铜箔复合而成。刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。请写出反应的离子方程式____________________。Cu放入0.1 mol/L FeCl3溶液中,反应一段时间后取出Cu片,溶液中Fe3+与Fe2+的物质的量浓度之比为4∶3,则反应后溶液中Cu2+与Fe3+的物质的量之比为(______)
A.3∶2 B.3∶8 C.4∶3 D.3∶4
(2)FeCl3在天然水中可生成氢氧化铁胶体,其沉降水中悬浮物的速度高于铝盐(如硫酸铝等),是城市污水及工业废水处理的高效絮凝剂。实验室制取氢氧化铁胶体的方法是________(填字母序号)。
A.将饱和的FeCl3溶液滴入沸水中,生成棕黄色液体即可
B.在FeCl3溶液中加入足量的NaOH溶液
C.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色液体
D.将饱和的FeCl3溶液滴入沸水,并继续煮沸至生成红褐色沉淀
证明此胶体已经制成的最简单方法为____________________________________。
(3)FeCl3可使湿润的淀粉碘化钾试纸变蓝,化学方程式如下:2FeCl3+2KI===2FeCl2+I2+2KI在上式中用双线桥法标出该反应电子转移的方向和数目__________________。向反应后的溶液中加入CCl4溶液,振荡、静置后会发现下层液体的颜色为 ________色,再将混合液倒入________(填仪器名称)中,将两层液体分离。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com