
| A、新制氯水中只含有Cl2和H2O分子 |
| B、加入AgNO3溶液有白色沉淀产生 |
| C、光照氯水有气泡逸出,久置的氯水,酸性增强 |
| D、饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法 |
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
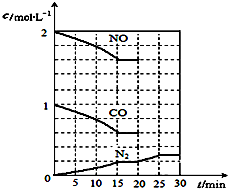 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3+HCl=NaCl+CO2↑+H2O |
| B、BaCO3+2HCl=BaCl2+H2O+CO2↑ |
| C、Na2CO3+H2SO4=Na2SO4+CO2↑+H2O |
| D、K2CO3+2CH3COOH=2CH3COOK+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、食盐中阴离子的结构示意图为: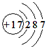 |
| B、蔗糖和醋酸都是弱电解质 |
C、“84消毒液”中有效成分NaClO的电子式为: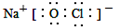 |
| D、明矾溶液水解可制得Al(OH)3胶体,用于杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol H2O的质量为18g?mol-1 |
| B、CO2的摩尔质量为44g |
| C、3.01×1023个SO2分子的质量为32g |
| D、64g氧气中含有2mol氧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
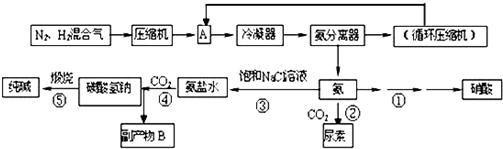
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210 | -253 | -78 |
| 沸点(℃) | -195 | -259 | -33 |
 反应②的化学方程式是
反应②的化学方程式是
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com