
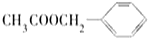 ���㷺�����ڿɿɡ����ȡ���ݮ�������У�������ʳ����ջ���Ʒ���㾫����֪��X�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ����ҵ�Ͽ���X�ͼױ��˹��ϳ����ᱽ��������ϳ�·�����£�
���㷺�����ڿɿɡ����ȡ���ݮ�������У�������ʳ����ջ���Ʒ���㾫����֪��X�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ����ҵ�Ͽ���X�ͼױ��˹��ϳ����ᱽ��������ϳ�·�����£�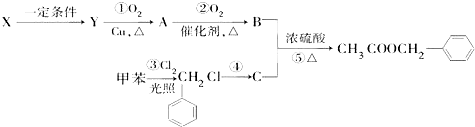
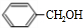 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$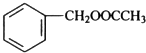 +H2O��
+H2O��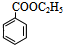 ��
�� ���� X�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ����XΪCH2=CH2��Xת���õ�Y��Y���������õ�B����B��C��Ӧ�õ����ᱽ��������BΪCH3COOH��CΪ���״����ṹ��ʽΪ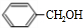 ����YΪCH3CH2OH��AΪCH3CHO���ݴ˽��н��
����YΪCH3CH2OH��AΪCH3CHO���ݴ˽��н��
��� �⣺X�IJ���������������һ�����ҵ�ʯ�ͻ�����չˮƽ����XΪCH2=CH2��Xת���õ�Y��Y���������õ�B����B��C��Ӧ�õ����ᱽ��������BΪCH3COOH��CΪ���״����ṹ��ʽΪ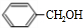 ����YΪCH3CH2OH��AΪCH3CHO��
����YΪCH3CH2OH��AΪCH3CHO��
��1��
�ʴ�Ϊ��2CH3CH2OH+O2$\stackrel{��}{��}$2CH3CHO��ȩ����
��2��A��������̼���Ʒ�Ӧ���ɶ�����̼������ȩ��̼���Ʋ���Ӧ���һ��ܣ����ô�����Һ������������ȩ����A��ȷ��
B���������������Ʒ�Ӧ��������������ȩ��NaOH��Һ���ܣ������𣬹�B����
C�������������ᷴӦ������������Ȼ��ȩ����Na��Ӧ������Һ�е�ˮ���Ʒ�Ӧ���������������𣬹�C����
D����ȩ��������Һ����������������������������Һ��Ӧ���������𣬹�D��ȷ��
�ʴ�Ϊ��AD��
��3����Ӧ��ΪCH3COOH�ͱ��״�����������Ӧ����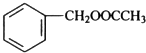 ����Ӧ�Ļ�ѧ����ʽΪ��CH3COOH+
����Ӧ�Ļ�ѧ����ʽΪ��CH3COOH+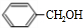 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$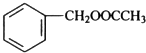 +H2O��
+H2O��
�ʴ�Ϊ��CH3COOH+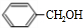 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$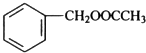 +H2O��
+H2O��
��4�������������������ᱽ������һ��ͬ���칹�壺�ٺ������ṹ���ھ������Ľṹ������������һ��ͬ���칹��Ϊ��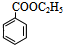 ��
��
�ʴ�Ϊ��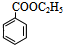 ��
��
���� ���⿼���л�����ƶϣ���Ŀ�Ѷ��еȣ�ע��������ᱽ�����Ľṹ�����ƶϣ���Ҫѧ���������չ����ŵ�������ת��������������ѧ���ķ���������������������������


 ͬ����ϰǿ����չϵ�д�
ͬ����ϰǿ����չϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�Ľṹ��ʽ��CH2 CH2 | B�� | ��ϩ�����ģ�ͣ�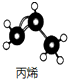 | ||
| C�� | ȩ���Ľṹ��ʽ��-COH | D�� | �ǻ��ĵ���ʽ��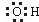 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ǿ������Һ��Mg2+��K+��SO42-��NO3- | |
| B�� | ʹ��̪���ɫ����Һ��Na+��Cu2+��HCO3-��NO3- | |
| C�� | 0.1mol•L-1AgNO3��Һ��H+��K+��SO42-��I- | |
| D�� | 0.1mol•L-lNaAlO2��Һ��H+��Na+��Cl-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 NH4++OH-��ʵ�����Ʊ�A���⻯��Ļ�ѧ����ʽΪCa��OH��2+2NH4Cl $\frac{\underline{\;\;��\;\;}}{\;}$ CaCl2+2NH3��+2H2O��
NH4++OH-��ʵ�����Ʊ�A���⻯��Ļ�ѧ����ʽΪCa��OH��2+2NH4Cl $\frac{\underline{\;\;��\;\;}}{\;}$ CaCl2+2NH3��+2H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2-��-3-��ϩ | B�� | 2-�һ����� | ||
| C�� | 3-��-1��3-����ϩ | D�� | 2��3-�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ϵͳ����������Ϊ2��2��4��4-�ļ�����
��ϵͳ����������Ϊ2��2��4��4-�ļ����� ��ϵͳ����������Ϊ2��2��3��3-�ļ�����
��ϵͳ����������Ϊ2��2��3��3-�ļ�����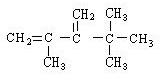 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaOH��Һ��ͨ�����SO2��SO2+2OH-�TSO32-+H2O | |
| B�� | п��ϡ���ᷴӦ��Zn+2H+�TZn2++H2�� | |
| C�� | ���Ȼ�淋���Һ�м�������ŨKOH��Һ�����ȣ�NH4++OH- $\frac{\underline{\;\;��\;\;}}{\;}$NH3•H2O | |
| D�� | ����ˮ��ͨ��SO2���壺Cl2+SO2+2H2O�T4H++2Cl-+SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��H2��=0.3 mol•L-1•min-1 | B�� | v��N2��=0.05 mol•L-1•s-1 | ||
| C�� | v��N2��=0.2 mol•L-1•min-1 | D�� | v��NH3��=0.3 mol•L-1•min-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com