
有关碱金属单质的叙述正确的是( )
A. 都可以保存在煤油中
B. 随电子层数增加,熔沸点逐渐降低
C. 都是银白色金属,质软,有延展性
D. 随电子层数增加,密度逐渐增大
科目:高中化学 来源: 题型:
可逆反应2NO(g)⇌O2(g)+N2(g);△H=﹣180kJ.mol﹣1,对此反应的逆反应,下列说法正确的是( )
|
| A. | 升高温度平衡常数K增大 |
|
| B. | 升高温度平衡常数K减小 |
|
| C. | 增大压力则平衡移动 |
|
| D. | 增大N2浓度,则NO分解率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
①可以判断该分解反应已经达到平衡的是________(填字母序号)。
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0 ℃时的分解平衡常数:____________。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量将________(填“增加”、“减少”或“不变”)。
④氨基甲酸铵分解反应的焓变ΔH____0(填“>”、“=”或“<”),熵变ΔS____0(填“>”、“=”或“<”)。
(2)已知:NH2COONH4+2H2ONH4HCO3+NH3·H2O,该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间的变化趋势如下图所示。
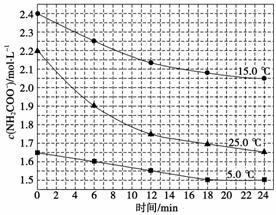
①计算25.0 ℃时,0~6 min氨基甲酸铵水解反应的平均速率:__________。
②根据图中信息,如何说明该水解反应速率随温度升高而增大:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应:2NO2⇌2NO+O2在固定体积密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2;
②单位时间内生成n mol O2 的同时,生成2n mol NO;
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2:2:1的状态;
④混合气体的颜色不再改变的状态;
⑤混合气体的密度不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态.
|
| A. | ①④⑥ | B. | ②③⑤ | C. | ①③④ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
铝合金是制造飞机、汽车等的常用材料.下列关子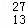 Al的叙述正确的是( )
Al的叙述正确的是( )
A. 质子数是27 B. 中子数是27 C. 电子数是13 D. 质量数是13
查看答案和解析>>
科目:高中化学 来源: 题型:
有德国重离子研究中心人工合成的第112号元素的正式名称为“Copernicium”,相应的元素符号位“Cn”.该元素的名称是为了纪念天文学家哥白尼而得名.该中心人工合成Cn的过程可表示为: Zn+
Zn+ ═
═
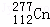 +
+ 下列叙述中正确的是( )
下列叙述中正确的是( )
A. 上述合成过程中属于化学变化
B. Cn元素的相对原子质量为277
C.  Cn的原子核内中子数比质子数多53
Cn的原子核内中子数比质子数多53
D. Cn元素位于元素周期表的第六周期,是副族元素
查看答案和解析>>
科目:高中化学 来源: 题型:
卤族元素随核电荷数的增加,下列叙述正确的是( )
A. 单质的颜色逐渐加深
B. 气态氢化物的稳定性逐渐增强
C. 单质的熔点逐渐升高
D. 单质的氧化性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
|
| A. | 2mol CH4的质量和O2的摩尔质量都是32g |
|
| B. | 1mol任何气体中都含有相同的原子数 |
|
| C. | 0.5molNaCl约含有6.02×1023个离子 |
|
| D. | 1mol/LKCl溶液中含有溶质1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
诺贝尔化学奖获得者泽维尔研究了氢气和二氧化碳的反应:H 2 +CO 2 ====CO+H 2 O,此反应在一定条件下经历了一个相对长的中间状态HCOOH。下列叙述正确的是( )
A.H 2 的还原性一定比CO强
B.CO还原性一定比H 2 强
C.反应条件对物质的还原性存在影响
D.以上反应不是氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com