
����Ŀ��A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������A��Eͬ���壬AԪ�ص�ԭ�Ӱ뾶��С��BԪ��ԭ�ӵ��������������ڲ��������2����CԪ��ԭ�ӵĵ��Ӳ���Ϊn������������Ϊ2n+1��A��B��C��Eÿ��Ԫ�ض�����DԪ��������ֻ��������ϵij�������� �ش��������⣺
��1��д�����и�Ԫ�ط��ţ�C___________ E____________
��2��A��C�γɵ��������ĵ���ʽΪ___________��A��D��ԭ����1:1�γɵĻ�����ĽṹʽΪ___________��
��3����֪�� BA3DA(g)+A2D(g)=BD2(g)+3A2(g) ��H= +49��0kJ��mol
BA3DA(g)+1��2D2(g)=BD2(g)+2A2(g) ��H = һ192��9kJ��mol
��д������̬BA3DA��ȫȼ��������̬A2D���Ȼ�ѧ����ʽ(���Ƴ���Ԫ�ط���д����ͬ)
______________________________________________________________��
���ø�ȼ�շ�Ӧ��Ƴɵ�ȼ�ϵ�����õ��ƹ㣬��д����ȼ�ϵ�ظ����缫��Ӧʽ(�������ҺΪKOH)��___________________________________________��
���𰸡�N Na ![]() H-O-O-H CH3OH��g��+ 3/2O2(g) �� CO2(g)+2H2O(g) ��H=-676.7kJ��mol-1 CH3OH-6e-+8OH-= CO32-+6H2O
H-O-O-H CH3OH��g��+ 3/2O2(g) �� CO2(g)+2H2O(g) ��H=-676.7kJ��mol-1 CH3OH-6e-+8OH-= CO32-+6H2O
��������
AԪ�ص�ԭ�Ӱ뾶��С����֪A����Ԫ�أ�BԪ��ԭ�ӵ��������������ڲ��������2�������ݶ�����Ԫ�ص�ԭ�ӽṹʾ��ͼ��֪��B��̼Ԫ�أ�CԪ��ԭ�ӵĵ��Ӳ���Ϊn������������Ϊ2n+l�����������Ķ�����Ԫ��ֻ�е�Ԫ�أ������ֶ�����Ԫ�أ�ԭ��������������A��Eͬ���壬��E����Ԫ�أ�A��B��C��Eÿ��Ԫ�ض�����DԪ��������ֻ��������ϵij��������D�ǵ�Ԫ������Ԫ��֮���Ԫ�أ�����ϵ�ֻ����Ԫ�أ��ݴ˷�������
��������������֪��
��1��CΪN��EΪNa��
��2��A��C�γɵ�����⻯��Ϊ�����������ʽΪ��![]() ��H��O�γɵ�ԭ�Ӹ�����Ϊ1:1������ΪH2O2����ṹʽΪ��H-O-O-H��
��H��O�γɵ�ԭ�Ӹ�����Ϊ1:1������ΪH2O2����ṹʽΪ��H-O-O-H��
��3��AΪH��BΪC��CΪN��DΪO��EΪNa���������Ȼ�ѧ����ʽ�ɸ�дΪ��
CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ��H= +49.0kJ/mol ��
CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ��H = һ192.9kJ/mol �ڣ���
O2(g)=CO2(g)+2H2(g) ��H = һ192.9kJ/mol �ڣ���
��![]() 3-��
3-��![]() 2��CH3OH��g��+ 3/2O2(g) =CO2(g)+2H2O(g) ��H=-676.7kJ��mol-1���ʴ�Ϊ��CH3OH��g��+ 3/2O2(g)=CO2(g)+2H2O(g) ��H= -676.7kJ��mol-1��
2��CH3OH��g��+ 3/2O2(g) =CO2(g)+2H2O(g) ��H=-676.7kJ��mol-1���ʴ�Ϊ��CH3OH��g��+ 3/2O2(g)=CO2(g)+2H2O(g) ��H= -676.7kJ��mol-1��
ȼ�ϵ�ظ���Ϊ�״�ʧ���ӷ�����������Ӧ����缫��ӦʽΪCH3OH-6e-+8OH-= CO32-+6H2O��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A.Na2S��ˮ�⣺S2��+ 2H2O![]() H2S + 2OH
H2S + 2OH
B.NaHCO3��ˮ��Һ�еĵ��룺HCO3+ H2O![]() H2 CO3+ OH
H2 CO3+ OH
C.NH4Cl��ˮ�⣺NH4+ + H2O![]() NH3��H2O + OH
NH3��H2O + OH
D.��������Һ��̼��������Һ��ϣ� Al3+ + 3HCO3 = Al(OH)3��+3CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������㶨���ܱ������м���1mol X�����2mol Y���壬�������·�Ӧ��X(g)��2Y(g)![]() 2Z(g)���˷�Ӧ�ﵽƽ��ı�־��
2Z(g)���˷�Ӧ�ﵽƽ��ı�־��
A.������ѹǿ����ʱ��仯
B.v��(X)=2v��(Y)
C.������X��Y��Z��Ũ��֮��Ϊ1�U2�U2
D.��λʱ������0.1mol Xͬʱ����0.2mol Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ͼ������ij�¶���![]() ��
��![]() �ֱ�����Һ�дﵽ�����ܽ�ƽ��ı���ҺpH������������Ũ�ȵı仯ͼ��ͼ���dz�������100mL
�ֱ�����Һ�дﵽ�����ܽ�ƽ��ı���ҺpH������������Ũ�ȵı仯ͼ��ͼ���dz�������100mL![]() ��Һ����μ���
��Һ����μ���![]() ��Һ�������Һ��pH�仯ͼ����ͼ��ʾ���Ʋ�Ľ����������
��Һ�������Һ��pH�仯ͼ����ͼ��ʾ���Ʋ�Ľ����������
ͼ��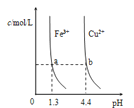 ͼ��
ͼ��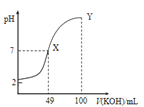
A.��ͼ��֪��![]()
B.��ͼ��֪��a��b����Һ��![]() ��b��Ĵ�
��b��Ĵ�
C.��ͼ��֪��HAΪǿ��
D.��ͼ��֪��Y���Ӧ����Һ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������ܱ������ڷ���ij������ϵ��Ӧ��������ͼ��ա�
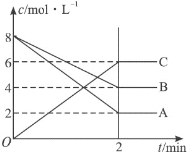
��1����Ӧ����___����������____��
��2����2min��A��ƽ����Ӧ����Ϊ___mol��L-1��min-1��
��3���÷�Ӧ�Ļ�ѧ����ʽ��__![]() ___��
___��
��4��д���˷�Ӧ��ƽ�ⳣ������ʽ___��������A��B��C��ʾ��������ѹǿ��ƽ����___����������������������Ӧ�����ƶ���K___������������������С����������������
��5��ת����Ϊ�ѷ�Ӧ�����ʵ������ʼ���ʵ�����ֵ��B��ת����Ϊ___���������¶ȣ�B��ת�������ӣ�������Ӧ��___��������������������������
��6��2���Ӻ��ijʱ�̣�t1���ı�ijһ����ʹƽ���ƶ���������ͼ��ʾ��������___��
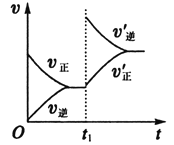
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ij�¶���0.5mol��L-1 HNO2�������ᣩ��Һ��pHԼΪ2��
��1��д��HNO2�ĵ��뷽��ʽ___��
��2������Һ��ˮϡ����10����c(NO2-)___������������������С����������������n(H+)___������������������С����������������pH���䷶Χ��___��
A.1��2 B.2��3 C.3��4 D.4��5
��3���ֱ�ȡͬŨ��ͬ����������������ᣬ��ͬ���IJ���������NaOH��Һ��Ӧ����÷�Ӧ��Һ������¶�����Ҫ���������ᣬ˵�����ܵ�ԭ��___��
��4��0.1mol��L-1 NaNO2��ҺpH___7��������������������������������Һ�к���___�ַ��ӣ���Һ��c(Na+)___c(NO2-)���������������������������������д�ʩ�������Һ��c(OH-)����___��
A.�ʵ������¶� B.����ѹǿ C.��ˮ D.����NH4Cl���� E.����Na2CO3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�������γɶ��������磺[Fe(CN)6]4- ��Fe(SCN)3 �ȡ�
��1����̬��ԭ�Ӻ�������Ų�ʽΪ________________.
��2����ѧ�о������� TiO2 ��������ɽ���ˮ�� CN- ת��ΪOCN-������������Ϊ N2 ��CO2��OCN- ������Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ_________��
��3���� CN- ��Ϊ�ȵ������һ�ַ���Ϊ________________���ѧʽ����1mol Fe��CN��63- �к���![]() ������ĿΪ________________��
������ĿΪ________________��
��4��������һ�������Fe(CO)5 �۵�Ϊ ��20.5�����е�Ϊ 103����������CCl4���ݴ˿����ж�Fe(CO)5 ��������________________��������ͣ���
��5�������Ͻ��һ�־����������������ṹ���侧���ɿ����� 8 ��С���������ṹ�������ɡ���֪С��������ͼ��ʾ���úϽ�Ļ�ѧʽΪ________________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ�����ӽ���Ĥ����ⱥ��ʳ��ˮԭ��ʾ��ͼ������˵����ȷ����

A.��E���ݳ��������� Cl2
B.ÿ���� 22.4 L Cl2��ͬʱ����2 mol NaOH
C.��B�ڼ��뺬����NaOH��ˮ��Һ����ǿ������
D.������Na2CO3��NaOH��BaCl2��������Լ���ȥ����ˮ��Ca2+��Mg2+��Fe3+��SO42��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ����
A.ͭͶ��Ũ�����У�Cu + 2NO![]() + 2H+ = Cu2+ + 2NO��+ H2O
+ 2H+ = Cu2+ + 2NO��+ H2O
B.������Ͷ��ϡ�����У�Al2O3 + 6H+ =2Al3+ + 3H2O
C.�ƺ�ˮ��Ӧ��Na + H2O = Na+ + OH�� + H2��
D.��ʳ���ܽ�������þ��Mg(OH)2��2H+=Mg2++2H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com