
分析 (1)有相同质子数,不同中子数的原子互为同位素;
(2)质量数等于质子数与中子数之和;
(3)元素在周期表中原子序数=质子数;
(4)元素的化学性质与元素核外电子排布有关,主要主要决定于最外层电子数.
解答 解:(1)同位素是质子数相同,而中子数不同的原子,同位素主要决定于质子数和中子数,
故答案为:质子数和中子数;
(2)果忽略电子的质量,将核内所有质子和中子的相对质量取近似值加起来,所得的数值叫做质量数,因此,在原子中,质量数等于质子数与中子数之和,即质量数决定于质子数和中子数,
故答案为:质子数和中子数;
(3)按照元素在周期表中的顺序给元素编号,就得到原子序数,而元素在周期表中是按照质子数排列的,即质子数=原子序数,故原子序数决定于质子数,
故答案为:质子数;
(4)在原子结构中,最外层电子数目决定了元素的主要化学性质,如最外层电子数小于4的容易失电子,大于4的容易得电子,
故答案为:最外层电子数.
点评 本题考查有关同位素、质量数、原子序数、元素的化学性质的决定因素,掌握相关概念是解答关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:推断题
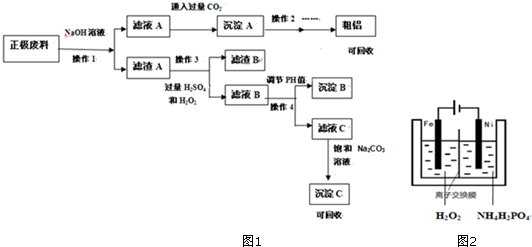
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{A}$(A-Z+2m)mol | B. | $\frac{a}{A}$(A+2m)mol | C. | $\frac{a}{A+m}$(A-Z+3m)mol | D. | $\frac{a}{A+3m}$ (A-Z+2m)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | Z | |
| R | |||
| W | |||
| J |
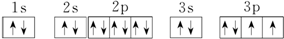 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
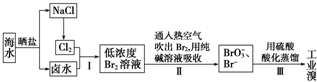
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
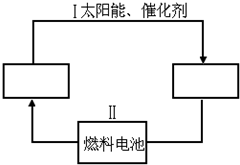 能源可化分为一级能源和二级能源.自然界以现成方式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,而如何快速制取出大量的氢气则成为发展氢能源的主要问题.
能源可化分为一级能源和二级能源.自然界以现成方式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,而如何快速制取出大量的氢气则成为发展氢能源的主要问题. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 相对密度(20℃) | 熔点 | 沸点 | 溶解性 | |
| A | 0.7893 | -117.3°C | 78.5°C | 与水以任意比混溶 |
| B | 0.7137 | -116.6°C | 34.5°C | 不溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com