
25 ��ʱ����Ũ��Ϊ0.100 0 mol��L��1��NaOH��Һ�ζ�20.00 mLŨ�Ⱦ�Ϊ0.100 0 mol��L��1��������HX��HY��HZ���ζ�������ͼ��ʾ������˵����ȷ����(����)��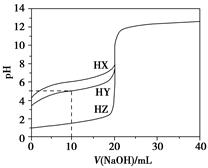
| A������ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳��HZ��HY��HX |
| B�����ݵζ����ߣ��ɵ�Ka(HY)��10��5 |
| C��������HX��HY��Һ�������Ϻ���NaOH��Һ�ζ���HXǡ����ȫ��Ӧʱ��c(X��)��c(Y��)��c(OH��)��c(H��) |
D��HY��HZ��ϣ��ﵽƽ��ʱc(H��)�� ��c(Z��)��c(OH��) ��c(Z��)��c(OH��) |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�������pH��ͬ�İ�ˮ��NaOH��Һ������˵����ȷ����
| A���ֱ��ˮϡ����ͬ�ı�����ϡ�ͺ�����ҺpH����ͬ |
| B��NaOH��Һ��ˮ���������c(OH��)��С |
| C���õ�Ũ�ȵ�������ȫ�кͣ��������������� |
| D����������NH4Cl(s)��pH����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��������Ũ�ȵ�HCN��Һ��NaCN��Һ�������ϣ����Һ�Լ��ԣ�����˵�������
| A��c��CN���� ��c��Na+����c��H+����c��OH���� |
| B��c��Na+����c��CN������c��OH������c��H+�� |
| C��c��Na+��+ c��H+��= c��CN����+ c��OH���� |
| D��2c��OH����+ c��CN����=2c��H+��+c��HCN�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��25��ʱ��FeS��CuS���ܶȻ�������Ksp���ֱ�Ϊ6��3��10��18��1��3��10��36������ʱ����
�й�˵����ȷ���ǣ�������
| A����ȥ��ҵ��ˮ�е�Cu2������ѡ��FeS�������� |
| B����H2S�ı�����Һ��ͨ������SO2������Һ��������ǿ |
| C����ΪH2SO4��ǿ�ᣬ���Է�Ӧ��CuSO4ʮH2S��CuS����H2SO4���ܷ��� |
| D����������CuSO4�ܽ���0.1 mol��L��H2S��Һ�У���Һ��Cu2�������Ũ��Ϊ1.3��10��35mol��L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ���¶��µ����ܵ����AmBn��ˮ��Һ�дﵽ�����ܽ�ƽ��ʱ,��ƽ�ⳣ��Ksp=cm(An+)��cn(Bm-),��Ϊ���ܵ���ʵ��ܶȻ���25 ��ʱ,��AgCl�İ�ɫ����Һ��,���μ����Ũ�ȵ�KI��Һ��Na2S��Һ,�۲쵽���������ȳ��ֻ�ɫ����,������ɺ�ɫ��������֪�й����ʵ���ɫ���ܶȻ�����:
| ���� | AgCl | AgI | Ag2S |
| ��ɫ | �� | �� | �� |
| Ksp(25 ��) | 1.8��10-10 | 1.5��10-16 | 1.8��10-50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵����ȷ���� (����)��
| A����ӦA(g)??2B(g)����H��������Ӧ�Ļ��ΪEa kJ��mol��1���淴Ӧ�Ļ��ΪEb kJ��mol��1����H��(Ea��Eb)kJ��mol��1 |
| B����״���£���0.1 mol��L��1�İ�ˮ�м��������Ȼ�茶��壬�������ҺpH��7����c(NH4+)��c(Cl��) |
| C��������пͭ�Ͻ���100 mL pH��1ϡ���ᷴӦ����Ӧ3 sʱ���pH��2�����跴Ӧǰ����Һ��������ֲ��䣬��3 s�ڲ���������ƽ��������33.6 mL��s��1 |
D����Ũ��Ϊ0.1 mol��L��1 HF��Һ��ˮ����ϡ�����У�����ƽ�ⳣ��Ka(HF)���ֲ��䣬 ʼ�ձ������� ʼ�ձ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����Һ�������25 �棬�й�������ȷ����( )
| A��Na2CO3��Һ�У�c(OH��)��c(H+)��c(HCO3��) +2c(H2CO3) |
| B��AgCl��ͬŨ�ȵ�MgCl2��KCl��Һ�е��ܽ����ͬ |
| C����ϡ��ˮ��μ���ϡ�����У�����ҺpH =7ʱ��c(SO42��) >c(NH4+) |
| D��Na2S��Һ��ˮϡ�ͺָ���ԭ�¶ȣ�pH��Kw����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����ʱ��0.1 mol��L��1��HA��Һ��pH��3�������Һ����μ���NaOH��Һ���ڵμӹ����У��й�������ȷ���� (����)��
| A��ԭHA��Һ�У�c(H��)��c(OH��)��c(A��) |
| B��������������NaOH��Һʱ���ٽ���HA�ĵ��룬��Һ��pH���� |
| C����ǡ����ȫ�к�ʱ����Һ������ |
| D����NaOH��Һ����ʱ�����ܳ��֣�c(A��)>c(Na��)>c(OH��)>c(H��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij�¶��£�0.1 mol��L��1 NaHCO3��ҺpH��10�������ж���ȷ����(����)��
| A��c(OH��)��10��4 mol��L��1 |
| B����������NaOH���壬c(Na��)��c(HCO3��)������ |
| C��c(Na��)��c(H��)��c(HCO3��)��c(OH��) |
| D��c(Na��)��c(HCO3��)��c(CO32��)��c(H2CO3) |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com