
【题目】a、b、c、d、e为原子序数依次增大的五种常见短周期元素,可组成一种化合物A,其化学式为ba4d(ec4)2。A能够发生如下转化关系:

己知C的分子式为ba3,能使湿润的红色石蕊试纸变蓝。则下列说法正确的是
A.原子半径b>c
B.e的氧化物的水化物为强酸
C.化合物A为共价化合物
D.元素非金属性强弱c<e
【答案】A
【解析】
A和氢氧化钠溶液反应生成B和C,C为气体,C的分子式为ba3,能使湿润的红色石蕊试纸变蓝,根据化学式可推断C为氨气,B为白色沉淀,继续加入氢氧化钠溶液沉淀溶解,则B可推断为氢氧化铝,A中加入酸化的氯化钡溶液形成白色沉淀,则A中含有硫酸根离子,根据以上推断,A为NH4Al(SO4)2,a为H元素,b为N元素,c为O元素,d为Al元素,e为S元素,据此分析解答。
A.b为N元素,c为O元素,同周期元素随核电荷数增大,半径逐渐减小,则原子半径b>c,故A正确;
B.e为S元素,S的氧化物的水化物有硫酸和亚硫酸,亚硫酸是弱酸,故B错误;
C.A为NH4Al(SO4)2,是离子化合物,故C错误;
D.c为O元素,e为S元素,同主族元素随核电荷数增大非金属性逐渐减弱,元素非金属性强弱c>e,故D错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】N2O5在一定温度下可发生反应:2N2O5(g)![]() 4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
4NO2(g)+O2(g) ΔH>0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
时间/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/(mol·L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法正确的是( )
A.500s内NO2的生成速率为2.96×10-3mol/(L·s)
B.T1温度下该反应平衡时N2O5的转化率为29.6%
C.平衡后,其他条件不变,将容器体积变为原来的![]() ,则c(N2O5)<5.00mol/L
,则c(N2O5)<5.00mol/L
D.T1、T2温度下的平衡常数分别为K1、K2,若T1>T2,则K1>K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,向20 mL 0.1 mol·L-1 H2A溶液中滴加0.1 mol·L-1的NaOH溶液,有关粒子物质的量的变化如图所示。下列说法正确的是

A.II表示微粒A2-的物质的量的变化曲线
B.H2A在水中的第一步电离方程式为H2A![]() A2-+2H+
A2-+2H+
C.![]() 的值随着V[NaOH(aq)]的增大而减小
的值随着V[NaOH(aq)]的增大而减小
D.V[NaOH(aq)]=20 mL时,溶液中存在关系:c(HA-)+c(A2-)+c(H2A)=0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明代《天工开物》记载“火法”冶炼锌: “炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”(注:炉甘石的主要成分为碳酸锌,泥罐中掺有煤炭)。下列说法不正确的是
A. 倭铅是指金属锌和铅的混合物
B. 煤炭中起作用的主要成分是C
C. 冶炼Zn的反应方程式为:ZnCO3+2C![]() Zn+3CO↑
Zn+3CO↑
D. 该冶炼锌的方法属于热还原法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M、N分子的模型如图所示,其中不同颜色的球表示不同的原子,原子之间的化学键可以是单键、双键。下列说法错误的是
M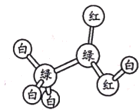 N
N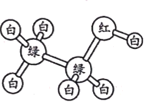
A.M与HCOOCH3互为同分异构体
B.N的官能团为羟基
C.在与钠的反应中N放出气泡比M快
D.N能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热△//=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△=2×(-57.3)kJ/mol
B.需要加热才能发生的反应一定是吸热反应
C.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0kJ/mo1
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.H2(g)+I2(g)![]() 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
B.C(s)+H2O(g)![]() H(g)+CO(g),碳的质量不再改变说明反应已达平衡
H(g)+CO(g),碳的质量不再改变说明反应已达平衡
C.若在恒温恒容容器内,压强不再随时间变化能说明反应2A(?)+B(g)![]() 2C(?)已达平衡,则A、C不能同时是气体
2C(?)已达平衡,则A、C不能同时是气体
D.1 mol N2和3 mol H2反应达到平衡时H2转化率为10%,放出的热量为Q1;在相同温度和压强下,当2 mol NH3分解为N2和H2的转化率为10%时,吸收的热量为Q2,Q2不等于Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,将2.0molA(g)和2.0molB(g)充入体积为1L的密闭容器中,在一定条件发生下述反应:A(g)+B(g)![]() 2C(g)+D(s) △H<0;t时刻反应达到平衡时,C(g)为2.0mol。下列说法正确的是( )
2C(g)+D(s) △H<0;t时刻反应达到平衡时,C(g)为2.0mol。下列说法正确的是( )
A.t时刻反应达到平衡时,A(g)的体积分数为20%
B.T℃时该反应的化学平衡常数K=2
C.t时刻反应达到平衡后,缩小容器体积,平衡逆向移动
D.T℃时,若将A(g)、B(g)各1.0mol充入同样容器,平衡后,a(A)为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2C2O4(草酸)为二元弱酸,在水溶液中H2C2O4、HC2O4-和C2O42-物质的量分数与pH关系如图所示,下列说法不正确的是
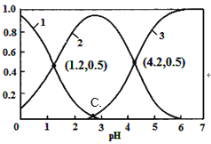
A.根据图中数据计算可得C点溶液pH为2.7
B.向草酸溶液中滴加氢氧化钠溶液至pH为4.2时c(Na+)+c(H+)=3c(C2 O42-)+c(OH-)
C.0.1 mol·L-1NaHC2O4溶液中c(Na+)>c(HC2O4-)>c(H+)>c(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HC2O4-)> c(C2 O42-) >c(H+)=c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com