
| A. | 该反应体现了浓H2SO4的酸性和强氧化性 | |
| B. | 被还原的硫酸为$\frac{V}{22.4}$mol | |
| C. | 反应结束后两种反应物均有剩余 | |
| D. | 参加反应的铜为0.18mol |
分析 A.该反应的硫酸中部分S元素化合价不变、部分S元素化合价由+6价变为+4价;
B.被还原硫酸的物质的量与二氧化硫的物质的量相等,根据S元素守恒计算被还原硫酸的物质的量;
C.加热条件下,浓硫酸和Cu反应,但稀硫酸和Cu不反应;
D.根据二氧化硫和Cu之间的关系式计算.
解答 解:A.该反应的硫酸中部分S元素化合价不变、部分S元素化合价由+6价变为+4价,参加反应的浓硫酸化合价不变的部分体现酸性,化合价降低的部分体现强氧化性,故A正确;
B.被还原硫酸的物质的量与二氧化硫的物质的量相等,根据S元素守恒得被还原硫酸的物质的量=$\frac{VL}{22.4L/mol}$=$\frac{V}{22.4}$mol,故B正确;
C.加热条件下,浓硫酸和Cu反应,但稀硫酸和Cu不反应,随着反应进行,浓硫酸变为稀硫酸时停止反应,所以反应结束后两种反应物均有剩余,故C正确;
D.发生的反应为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,因为浓硫酸变为稀硫酸时停止反应,硫酸有剩余,所以不能根据浓硫酸计算消耗Cu的量,可以根据二氧化硫计算Cu的消耗量,n(Cu)=n(SO2)=$\frac{VL}{22.4L/mol}$=$\frac{V}{22.4}$mol,故D错误;
故选D.
点评 本题考查氧化还原反应有关计算,侧重考查学生分析计算能力,注意:浓硫酸和Cu在加热条件下反应而稀硫酸不反应,易错选项是D.


科目:高中化学 来源: 题型:选择题
| A. | 氯胺水解产物最初为羟胺(NH2OH)和HCl | |
| B. | 氯胺在一定条件下可与乙烯加成得H2NCH2CH2Cl | |
| C. | 氯胺的消毒原理与漂白粉相似 | |
| D. | 氯胺的电子式为 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X 的能量一定高于 M | |
| B. | X 和 Y 的总能量一定高于 M 和 N 的总能量 | |
| C. | Y 的能量一定高于 N | |
| D. | 因为该反应是放热反应,故不必加热反应就一定能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
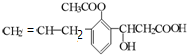 ,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦缩聚 ⑧中和 则( )
,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦缩聚 ⑧中和 则( )| A. | 除①⑥外均能 | B. | 除①⑦外均能 | C. | 除⑥⑦外均能 | D. | 以上反应均能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH2-CH2-CH2-CH2Cl | B. | 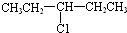 | ||
| C. | 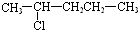 | D. | 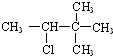 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下测得1molN2的质量为28g | |
| B. | 用量筒测得排水法收集制得的氢气体积为50.28mL | |
| C. | 用两只250mL的容量瓶配制0.1mol/L500mL的NaOH溶液 | |
| D. | 用托盘天平称得2.5g胆矾,受热充分失水后,固体质量减轻1.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的 金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对;有 |
| B | 常温下铁与稀硫酸反应 生成氢气 | 高温下氢气能还原氧化 铁得到铁 | Ⅰ对;Ⅱ对;无 |
| C | 铁属于过渡元素 | 铁和铁的某些化合物可用作催化剂 | Ⅰ错;Ⅱ对;无 |
| D | 在空气中铁的表面能形 成致密的氧化膜 | 铁不能与氧气反应 | Ⅰ对;Ⅱ对;有 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com