
 某无色稀溶液X中,可能含有表所列离子中的某几种.
某无色稀溶液X中,可能含有表所列离子中的某几种.| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
| A. | 若Y是盐酸,则Oa段转化为沉淀的离子(表中,下同)只有AlO2- | |
| B. | 若Y是盐酸,则溶液中可能含有的阳离子是Al3+ | |
| C. | 若Y是NaOH溶液,则bc段反应的离子方程式为 Al(OH)3+OH-═AlO2-+2H2O | |
| D. | 若Y是NaOH溶液,则X溶液中只存四种离子是:Al3+、Fe3+、NH4+、Cl- |
分析 A.若Y是盐酸,SiO32-、AlO2-与盐酸反应都会生成沉淀;
B.若Y是盐酸,ab段沉淀的物质的量不变,则盐酸与CO32-反应,结合离子共存分析;
C.若Y是NaOH溶液,bc段沉淀减少,是氢氧化铝溶于过量的氢氧化钠;
D.若Y是NaOH溶液,则不能判断溶液中是否含有Na+.
解答 解:A.若Y是盐酸,SiO32-、AlO2-与盐酸反应都会生成沉淀,所以oa段转化为沉淀的离子有AlO2-和SiO32-,故A错误;
B.若Y是盐酸,ab段沉淀的物质的量不变,则盐酸与CO32-反应,所以溶液中一定有CO32-,CO32-与Al3+不能共存,所以不含有Al3+,故B错误;
C.若Y是NaOH溶液,bc段沉淀减少,是氢氧化铝溶于过量的氢氧化钠,则发生反应的离子方程式为:Al(OH)3+OH-═AlO2-+2H2O,故C正确;
D.若Y是NaOH溶液,则不能判断溶液中是否含有Na+,所以溶液中可能还有Na+,故D错误.
故选C.
点评 本题考查了离子之间的反应,根据图象分析出有哪些离子之间发生反应,结合离子共存来分析解答,题目难度中等,注意把握常见离子之间的反应.


 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:选择题
 向一定量的硫酸、硫酸铝、硫酸铁的混合溶液中逐滴加入NaOH溶液,生成沉淀量随NaOH溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向一定量的硫酸、硫酸铝、硫酸铁的混合溶液中逐滴加入NaOH溶液,生成沉淀量随NaOH溶液加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | a点对应的溶液:NH4+、Fe2+、Cl-、NO3- | |
| B. | b点对应的溶液:K+、Cl-、SCN-、MnO4- | |
| C. | c点对应的溶液:K+、Fe2+、Br-、NO3- | |
| D. | d点对应的溶液:Ba2+、HCO3-、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V正=0 | B. | V逆=0 | C. | V正=V逆≠0 | D. | V正=V逆=0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
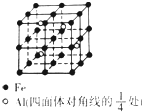 某宝石的主要成分是Al2O3,其中混有少量Mg、Ti、Fe等杂质而使其呈蓝色.
某宝石的主要成分是Al2O3,其中混有少量Mg、Ti、Fe等杂质而使其呈蓝色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuSO4溶液中加入过量氨水得到深蓝色溶液:Cu2++2OH-═Cu(OH)2↓ | |
| B. | 碳酸钠溶液中滴入酚酞试液,溶液变红:CO32-+2H2O?H2CO3+2OH- | |
| C. | FeCl2溶液中加入K3[Fe(CN)6]溶液,生成蓝色沉淀:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓ | |
| D. | 90℃时,测得纯水pH=6.7,pH<7的原因是:H2O(l)?H+(aq)+OH-(aq)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴加试剂 | 蒸馏水 | 盐酸 | 氯化铵溶液 |
| 现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上月考二化学试卷(解析版) 题型:选择题
下列关于物质分类的说法正确的是( )
A.SO2、CO、CO2都是酸性氧化物
B.BaSO4、Ca(OH)2、KNO3溶液都是电解质
C.纯碱、烧碱、碱石灰都是碱
D.稀豆浆、牛奶、淀粉溶液都是胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com