
| A. | 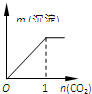 | B. | 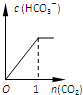 | C. | 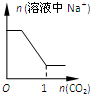 | D. | 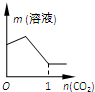 |
分析 碳酸钠饱和溶液中通入二氧化碳,发生反应Na2CO3+H2O+CO2=2NaHCO3,碳酸氢钠溶解度比碳酸钠的溶解度小,而且反应过程中又消耗了水,导致溶液中的溶剂质量减少,就会导致生成的碳酸氢钠过饱和而生成沉淀,据此解答.
解答 解:A.刚开始为饱和碳酸钠溶液,没有沉淀析出,通入二氧化碳少量时发生反应Na2CO3+H2O+CO2=2NaHCO3,但是碳酸氢钠还为达到饱和,所以不会有沉淀析出,一段时间后生成的碳酸氢钠增大,达到饱和开始产生沉淀,故A错误;
B.碳酸钠饱和溶液中通入二氧化碳,发生反应Na2CO3+H2O+CO2=2NaHCO3,碳酸氢根离子浓度增大,当生成的碳酸氢钠达到溶解度时,碳酸氢根离子浓度不再增大,通入二氧化碳的量小于1mol,故B错误;
C.饱和溶液中通入二氧化碳反应生成碳酸氢钠,继续通入,随着二氧化碳通入量增大,碳酸氢钠达到饱和,有沉淀析出,所以开始钠离子浓度不变,后来变小,最后碳酸钠完全转化为碳酸氢钠溶液,钠离子浓度又保持不变,故C正确;
D.碳酸钠饱和溶液中通入二氧化碳,发生反应Na2CO3+H2O+CO2=2NaHCO3,溶液质量增加,当通入二氧化碳反应生成的碳酸氢钠达到其溶解度时,再通入二氧化碳反应生成的碳酸氢钠不能溶解,溶液质量减小,最后变为饱和碳酸氢钠溶液后保持不变,故D正确;
故选:CD.
点评 本题考查了碳酸钠与碳酸氢钠的转化,明确二者化学性质及饱和溶液性质是解题关键,题目难度较大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4gNaOH固体所含电子总数为2NA | |
| B. | 22.4LC2H6所含化学键总数为7 NA | |
| C. | 常温常压下,14gC0、N2混合气体所含分子总数为NA | |
| D. | 0.1 mol-1LNH4C1溶液中,NH4+与Cl一数之和小于0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 实验室用图所示装置电解氯化铜溶液,实验中观察到碳(I)电极质量增加,碳(II)电极有气体放出.下列说法正确的是( )
实验室用图所示装置电解氯化铜溶液,实验中观察到碳(I)电极质量增加,碳(II)电极有气体放出.下列说法正确的是( )| A. | a为电源正极 | B. | 电极Ⅱ上发生还原反应 | ||
| C. | 电子流向:a→Ⅰ→Ⅱ→b | D. | 该装置将电能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
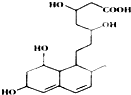
| A. | 含有两种官能团 | |
| B. | 能发生加成、酯化、氧化反应 | |
| C. | 1mol该物质与足量Na反应,产生2.5gH2 | |
| D. | 能使溴水和酸性高锰酸钾溶液褪色,褪色原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,SO2、Cl- K+、HCO3-可以大量共存 | |
| B. | 和FeCl3溶液反应的离子方程式:S2-+Fe3+═Fe2++S | |
| C. | 和少量盐酸反应的离子方程式:S2-+H+═HS- | |
| D. | 1L0.1mol•L-1该溶液和足量硫酸铜溶液反应生成16.0克Cu2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
| 向一定量铁粉中滴加稀盐酸 | 向一定量硫酸铜溶液中不断加入锌粉 | 加热一定量高锰酸钾固体 | 向一定量氢氧化钠 溶液中滴加稀盐酸 |
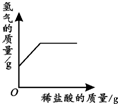 | 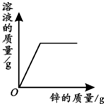 |  | 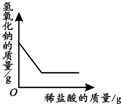 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
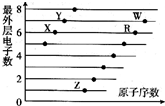
| A. | ZY、ZW的水溶液都显酸性 | |
| B. | 原子半径大小:W>R>X,离子半径大小:Z+>R2->W->Y- | |
| C. | W的氢化物水溶液的酸性比R的氢化物水溶液的酸性强,可证明非金属性:W>R | |
| D. | Z、X两种元素形成的Z2X、Z2X2为离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com