
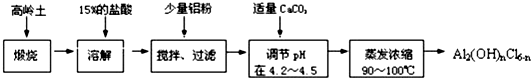
���� ��������ѧ���Ϊ��Al2O3��SiO2��Fe2O3�Լ��������ʺ�ˮ�֣������̿�֪�������������յĹ����пɳ�ȥ��ȼ�յ����ʺ�ˮ�֣��ı�������Ľṹ��ʹ���������ᣬ����������õ�����SiO2����Һ�к�Al3+��Fe3+���ӹ������ۣ��û�����������ȥ���������Ȼ�����Һ����̼��Ƶ�����Һ��pHֵ������Һ����Ũ���ü�ʽ�Ȼ�����
��1���������е��������������ᣬͨ�������ա��ı�������Ľṹ��ʹ���������
��2��������Һ���������������������ܼ�������֮�ͼ�����������ˮ������������������Һ�IJ���ѡ������������
��3�����ܽ⡱�����з��������������ᷴӦ�����Ȼ�����ˮ�����������ᷴӦ�����Ȼ�����ˮ��
��4��������������Ҫ�����ǣ���ȥ��Һ�е���Ԫ�أ�
��5�����Ƹ��¶���һ����Χ֮�䣬��ˮԡ���ȣ�
��6���������ͼӦ����ƫ�����Ρ�����������Ӧ���ɹ����Σ��ݴ���д���ӷ���ʽ��
��� �⣺��1���������е��������������ᣬ�����������յĹ����пɳ�ȥ��ȼ�յ����ʺ�ˮ�֣��ı�������Ľṹ��ʹ���������ᣬ���ԡ����ա���Ŀ�ĸı�������Ľṹ��ʹ���������ᣬ
�ʴ�Ϊ���ı�������Ľṹ��ʹ���������
��2����������������15%��������ˮ����Ϊm����Һ���������������������ܼ�������֮�ͣ���1.15g•cm-3��200ml+m����15%=1.15g•cm-3��200ml��30%����ã�m=230 g��������������15%����������㡢��ȡ���ܽ⡢ת�ơ����ݡ�����ǩ����Ҫ�õ����������ձ�ʢ����Һ�����������衢��Ͳ��ȡŨ����ȣ�
�ʴ�Ϊ��230���ձ�������������Ͳ��
��3�������������ᷴӦ�����Ȼ�����ˮ�����������ᷴӦ�����Ȼ�����ˮ�����ԡ��ܽ⡱���̷�Ӧ�����ӷ���ʽ�У�Al2O3+6H+=2Al3++3H2O��Fe2O3+6H+=2Fe3++3H2O��
�ʴ�Ϊ��Al2O3+6H+=2Al3++3H2O��Fe2O3+6H+=2Fe3++3H2O��
��4�������������ӷ�Ӧ�����������ӣ������������ӷ�Ӧ�û�������������������Ҫ�����ǣ���ȥ��Һ�е���Ԫ�أ�
�ʴ�Ϊ����ȥ��Һ�е������ӣ�
��5��ˮ�ķе�Ϊ100�棬������Ũ�����豣���¶���90��100�棬�ɲ��õļ��ȷ�����ˮԡ��
�ʴ�Ϊ��ˮԡ��
��6���������ͼӦ����ƫ�����Σ����ӷ�ӦΪ��Al2O3+2OH-=2AlO2-+H2O������������Ӧ���ɹ����Σ����ӷ�ӦΪ��SiO2+2OH-=SiO32-+H2O��
�ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��SiO2+2OH-=SiO32-+H2O��
���� ���⿼���˼�ʽ�Ȼ����Ʊ�������ʵ��̽��������ʵ���������������ʵ��ԭ���ǽ���ؼ�����Ŀ�Ѷ��еȣ���Ҫѧ���߱���ʵ�Ļ������Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
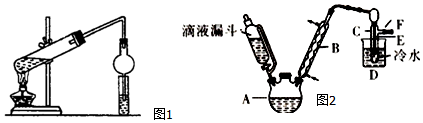
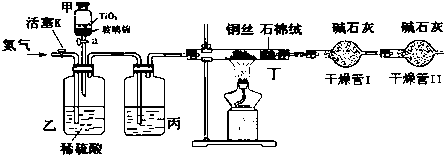
 ����ͼʾװ����ȡ���������������ƾ��Ƶ���ͼ�о�����ȥ��������գ�
����ͼʾװ����ȡ���������������ƾ��Ƶ���ͼ�о�����ȥ��������գ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| �Ҵ� | ������ | �� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | �����ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 1.44 | 3.1 |
| �е�/�� | 78.5 | 38.4 | 59 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
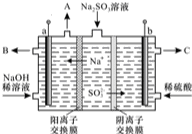 ���᳧�����ջ�����FeS2������ȡ���ᣬʵ�����������᳧��������Ҫ�ɷ���Fe2O3������FeS��SiO2���Ʊ��̷���
���᳧�����ջ�����FeS2������ȡ���ᣬʵ�����������᳧��������Ҫ�ɷ���Fe2O3������FeS��SiO2���Ʊ��̷���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
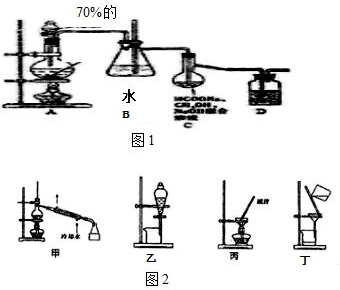
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
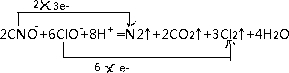 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
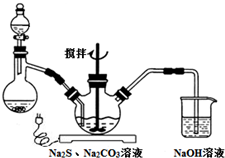 NaCNΪ�綾���ij��ȤС������ϵ�֪��ʵ�������NaCN��Һ����Na2S2O3��Һ���нⶾ���٣����ǿ�չ����������ʵ�飬�����Ҫ��ش����⣺
NaCNΪ�綾���ij��ȤС������ϵ�֪��ʵ�������NaCN��Һ����Na2S2O3��Һ���нⶾ���٣����ǿ�չ����������ʵ�飬�����Ҫ��ش����⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com