


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
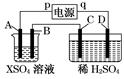
| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极产生气体 的体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极产生气体 的体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.10 mol·L-1AgNO3溶液 |
| B.0.10 mol·L-1ZnSO4溶液 |
| C.0.20 mol·L-1CuCl2溶液 |
| D.0.20 mol·L-1Pb(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
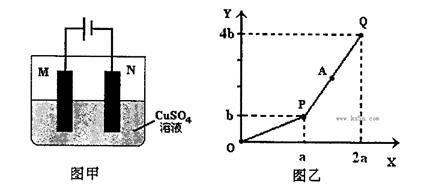
| A.电解过程中N电极表面先有红色物质生成,后有气泡产生 |
| B.A点所得溶液只需加入一定量的CuO固体就可恢复到起始状态 |
| C.Q点时M、N两电极上产生的气体在相同条件下体积相同 |
| D.若M电极材料换成Cu做电极,则电解过程中CuSO4溶液的浓度不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
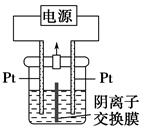
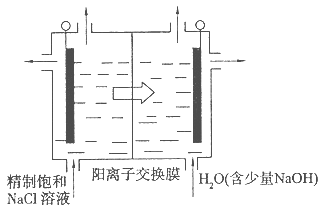
| A.右侧发生的电极反应式:2H2O+2e-=H2↑+2OH- |
| B.电解结束时,右侧溶液中含IO3— |
C.电解槽内发生反应的总化学方程式:KI+3H2O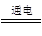 KIO3+3H2↑ KIO3+3H2↑ |
| D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
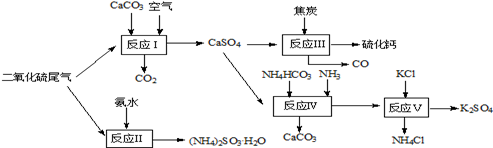
| A.滴有酚酞的NaOH溶液 | B.酸性KMnO4 |
| C.滴有淀粉的碘水 | D.BaCl2溶液. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 R2Cu(有机相)+2H+(水相)
R2Cu(有机相)+2H+(水相)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
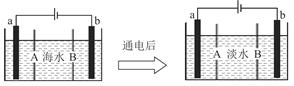
| A.B膜是阴离子交换膜 |
| B.通电后,海水中阳离子向a电极处运动 |
| C.通电后,a电极的电极反应式为4OH--4e-=O2↑+2H2↑ |
| D.通电后,b电极上产生无色气体,溶液中出现少量白色沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
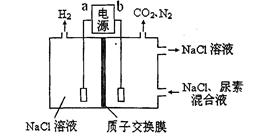
| A.电源的正极为b |
| B.尿素被氧化的化学方程式为CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl |
| C.电解结束后,阴极室溶液与电解前相比pH增大 |
| D.阳极收集到气体4.48 L(标准状况)时,被氧化的尿素为6.0 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com