
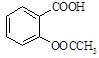 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下: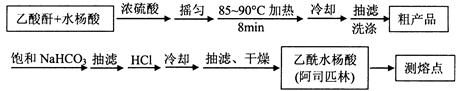
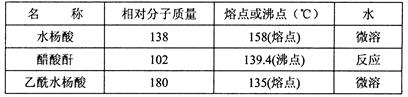
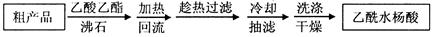
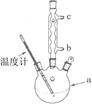
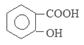 的相对分子质量为138,n(C7H6O3)=" 2.0" g÷138g/mol=0.0144mol;n(醋酸酐)=" (5.0" mL×1.08 g/cm3)÷102g/mol=0.0529mol.由于醋酸酐的物质的量大于水杨酸,所以得到的乙酰水杨酸应该按照水杨酸来计算。理论上得到乙酰水杨酸的质量为0.0144mol×180g/mol=2.6g.所以乙酰水杨酸的产率为(2.2g÷2.6g)×100%= 84.6%.
的相对分子质量为138,n(C7H6O3)=" 2.0" g÷138g/mol=0.0144mol;n(醋酸酐)=" (5.0" mL×1.08 g/cm3)÷102g/mol=0.0529mol.由于醋酸酐的物质的量大于水杨酸,所以得到的乙酰水杨酸应该按照水杨酸来计算。理论上得到乙酰水杨酸的质量为0.0144mol×180g/mol=2.6g.所以乙酰水杨酸的产率为(2.2g÷2.6g)×100%= 84.6%.

 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源:不详 题型:单选题
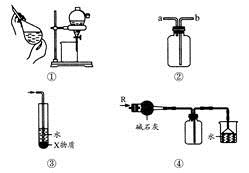
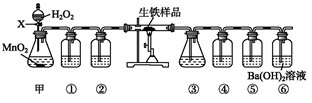
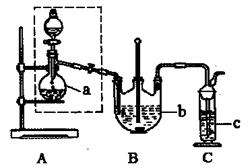
| A.装置①可用于分离C2H5OH和H2O的混合物 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
| D.装置④可用于干燥、收集NH3,并吸收多余的NH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
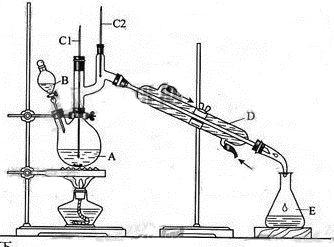
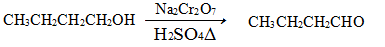
| | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 |
| 正丁醇 | 11.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 物 质 | 水 | 乙醇 | 乳酸 | 苯 | 乳酸乙酯 |
| 沸点/℃ | 100 | 78.4 | 122 | 80.10 | 154 |
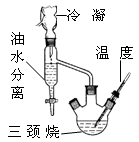
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 现象 | 解释 |
| A. | 向某溶液中加入盐酸 | 产生无色气体 | 溶液中一定含有CO32? |
| B. | 新制Fe(OH)2露置于空气中一段时间 | 白色固体迅速变为灰绿色,最终变为红褐色 | 说明Fe(OH)2易被氧化成Fe(OH)3 |
| C. | 在CuSO4溶液中加入KI溶液,再加入苯,振荡 | 上层呈紫红色,下层有白色沉淀生产 | 铜离子可以氧化碘离子,白色沉淀可能为CuI |
| D. | 向某无色溶液中滴加硝酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
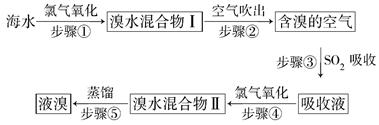
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
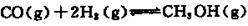
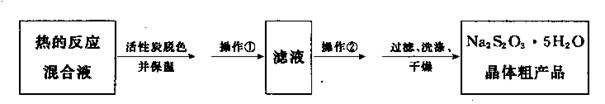
| A.用碱式滴定管盛装碘标准溶液 |
| B.用移液管移取25.00mL溶液于锥形瓶中,移液管的尖嘴和锥形瓶内壁要接触 |
| C.如果滴定终点没有控制好,碘标准溶液滴加过量,则必须重新进行滴定 |
| D.滴定过程中若剧烈摇动锥形瓶(溶液不外溅),则所测得的纯度将会偏高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 混合物 | 试剂 | 分离方法 |
| A | 乙烯(二氧化硫) | 溴水 | 洗气 |
| B | 溴苯(溴) | NaOH溶液 | 分液 |
| C | 苯(苯酚) | 加浓溴水 | 过滤 |
| D | 乙烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com